Mammakarzinom der Frau
Erstellung der Leitlinie
Stand: Januar 2013
1 Definition und Basisinformation
Das Mammakarzinom ist der häufigste maligne Tumor der Frau. Histologisch dominiert das invasive duktale Karzinom, gefolgt vom invasiven lobulären, dem tubulären, dem muzinösen und dem medullären Karzinom. Das duktale Carcinoma in situ (DCIS) und die atypische duktale Hyperplasie (ADH) sind Präkanzerosen. Thema dieses Kapitels ist das invasive Mammakarzinom der Frau. Das Mammakarzinom des Mannes wird in einem eigenen Kapitel abgehandelt (Mammakarzinom des Mannes).
1.1 Epidemiologie
In Deutschland wird die Zahl der Neuerkrankungen auf 74.500/Jahr geschätzt. Das Mammakarzinom macht 32% aller Krebserkrankungen bei Frauen aus mit einem mittleren Erkrankungsalter von 65 Jahren [1]. In der Schweiz wird die Zahl der Neuerkrankten auf 5.300/Jahr geschätzt, in Österreich lag sie im Jahr 2010 bei 5.105 Patientinnen [2]. Die Inzidenz war in Deutschland von 1980 bis 2000, in Österreich bis 1997, in der Schweiz bis 2008 stetig gestiegen. Insgesamt liegt die Lebenszeitwahrscheinlichkeit, an einem Mammakarzinom zur erkranken, für im Jahre 2008 geborene Mädchen bei 7%.
1.2 Risikofaktoren
Das Risiko, an einem Mammakarzinom zu erkranken, wird durch folgende Faktoren erhöht:
genetisch (ca. 5 % der Neuerkrankungen) [3]
vermehrtes Auftreten von Mamma- und / oder Ovarialkarzinom auf einer Seite der Familie (Kriterien des Deutschen Konsortiums für Familiären Brust- und Eierstockkrebs)
hereditäres Mamma- und Ovarialkarzinom mit Keimbahnmutationen im BRCA1 oder BRCA2 Gen
Peutz - Jeghers - Syndrom mit Keimbahnmutationen im STK11 Gen
Ataxia teleangiectasia mit Keimbahnmutationen im ATM Gen
Cowden - Syndrom mit Keimbahnmutationen in PTEN Genen
Keimbahnmutationen im CHEK-2 Gen
hormonell
frühe Menarche
späte Menopause
späte Gravidität
Adipositas, postmenopausale Gewichtszunahme
Hormonersatz - Therapie (HRT) postmenopausal
toxisch
Strahlenexposition der Brust im Kindes-, Jugend- und frühen Erwachsenenalter
Rauchen
hoher Alkoholkonsum (RR 1,46 bei>45 g Alkohol/Tag) [4]
kontralaterales Mammakarzinom (Erstkarzinom)
2 Vorbeugung und Früherkennung
2.1 Vorbeugung
Die allgemeinen Empfehlungen zur Vorbeugung beziehen sich auf die bisher identifizierten, erworbenen Risikofaktoren:
Übergewicht und postmenopausale Gewichtszunahme vermeiden
regelmäßige körperliche Bewegung
nicht rauchen
Verzicht auf exzessiven Alkoholkonsum
Selektive Östrogenrezeptor-Modulatoren (SERM, z. B. Tamoxifen, Raloxifen o. a.) oder der Aromataseinhibitor Exemestan reduzieren das Risiko für die Entstehung eines Hormonrezeptor-positiven Mammakarzinoms [5]. Der Nutzen hängt vom Risikostatus, dem Alter und vom Risiko für Nebenwirkungen ab.
2.2 Früherkennung
Die Screening-Mammographie kann die Sterblichkeit an Brustkrebs vermindern [6]. Der Wert anderer Screening-Methoden (Tastuntersuchung, Ultrasonographie) ist nicht etabliert. Die Magnetresonanztomographie ist indiziert zur Früherkennung bei jungen Patientinnen mit hereditärem Mammakarzinom-Syndrom. Zu den Leistungen der gesetzlichen Krankenkassen in Deutschland und in Teilen der Schweiz im Rahmen der Krebs - Früherkennung für Frauen gehören
jährliche, manuelle Untersuchung der Brust durch einen Arzt ab dem 30. Lebensjahr
zweijährliche Mammographie zwischen 50 und 69 Jahren
Die gesetzlichen Voraussetzungen für das Mammographie - Screening - Programm wurden in Deutschland im Jahre 2002 geschaffen. Bei prämenopausalen Frauen ist der Zykluszeitpunkt, d. h. die erste Zyklushälfte zwischen dem 7.-14. Zyklustag, für die Planung der Mammographie zu berücksichtigen.
3 Klinisches Bild
Im Vordergrund stehen lokale Symptome der Brust wie tastbarer Knoten, Hautveränderung oberhalb des Tumors einschl. der sog. Orangenhaut (peau d‘orange), Einziehung der Haut, Veränderung der Kontur, Asymmetrie der Brust, Einziehung der Mamille, Sekretion oder Blutung aus der Mamille auf der betroffenen Seite, Rötung und Überwärmung bei inflammatorischem Mammakarzinom. Weitere lokale Symptome sind tastbar vergrößerte Lymphknoten in Axilla oder Supraklavikularregion. Selten ist das Bild des lokal sehr fortgeschrittenen Karzinoms mit Ausbreitung auf die Brustwand (cancer en cuirasse) und Ulzerationen. Allgemeinsymptome fehlen in frühen Stadien des Mammakarzinoms. In fortgeschrittenen Stadien kann es zu Gewichtsabnahme und Leistungsminderung kommen. Symptome aufgrund von Metastasen sind Schwellung des Arms durch Lymphödem bei Lymphknotenmetastasen der Axilla, Knochenschmerzen bei Skelettmetastasen, Husten und Dyspnoe bei pulmonaler und / oder pleuraler Metastasierung, Ikterus und Leberinsuffizienz bei fortgeschrittener Lebermetastasierung oder neurologische Symptome bei cerebraler Metastasierung.
4 Diagnose
4.1 Diagnostik
Der erste Schritt ist die Bestätigung der klinischen und / oder bildgebenden Verdachtsdiagnose, s. Tabelle 1 [7, 8, 9].
Untersuchung | Empfehlung | Anmerkung |
Mammographie bds. | Methode der ersten Wahl | |
Biopsie (Stanzbiopsie oder Vakuumbiopsie) | bei BI-RADS1IV oder V | |
Sonographie beider Mammae und der Axillae | Methode der ersten Wahl <40 Jahren | |
Magnetresonanztomographie bds. mit Kontrastmittel | keine Standarduntersuchung | MRT2erhöht die Detektionsrate zusätzlicher Läsionen und beeinflusst das operative Vorgehen, aber ohne Verbesserung der Prognose3 |
1BI-RADS - Breast Imaging Report and Data System des American College of Radiology,2MRT - Magnetresonanztomographie;3siehe Studienergebnisse Mammakarzinom
Nach Diagnose eines Mammakarzinoms ist eine gezielte Ausbreitungsdiagnostik (Staging) für Patientinnen mit Tumoren>pT2 >pN0 und bei klinischen Symptomen indiziert, s. Tabelle 2. Fernmetastasen können beim Mammakarzinom in fast allen Regionen des Körpers auftreten. Die häufigsten Lokalisationen sind Skelett, Leber und Lunge.
Verdacht | Untersuchung (1. Wahl) | Anmerkungen / Untersuchungen zur Bestätigung oder bei unklarem Befund |
Skelettmetastasen | Skelettszintigraphie | Röntgen, MRT |
Lebermetastasen | Sonographie Abdomen | CT Abdomen |
Lungenmetastasen | Röntgen Thorax in 2 Ebenen | CT Thorax |
ZNS Metastasen | CT oder MRT | nur bei klinischem Verdacht |
Die Positronenemissionstomographie (PET) gehört nicht zum Standard in der Primärdiagnostik des Mammakarzinoms. Der Einsatz der18FDG-PET-CT in der Ausbreitungsdiagnostik führt zu einer Stadienmigration ohne erwiesene Verbesserung der Prognose für die individuelle Patientin.
4.2 Klassifikation
4.2.1 Anatomische Klassifikation
Die Klassifikation nach der Größe des Primärtumors und dem Ausmaß der Metastasierung erfolgt auf der Basis der TNM Kriterien. Die Einteilung der Union Internationale Contre le Cancer (UICC) fasst diese Kriterien in Stadien zusammen, s. Tabelle 3.
Stadium | Primärtumor | Lymphknotenstatus | Fernmetastasen |
0 | Tis | N0 | M0 |
I | T1mic | N0 | M0 |
T1a (1 - 5 mm) | N0 | M0 | |
T1b (6 - 10 mm) | N0 | M0 | |
T1c (11 - 20 mm) | N0 | M0 | |
IIA | T0, T1mic, T1 | N1 | M0 |
T2 | N0 | M0 | |
IIB | T2 | N1 | M0 |
T3 | N0 | M0 | |
IIIA | T0, T1mic, T1, T2 | N2 | M0 |
T3 | N1 | M0 | |
IIIB | T4 | N0 - 2 | M0 |
IIIC | alle T | N3 | M0 |
IV | alle T | alle N | M1 |
4.2.2 Histologischer Grad
Die histopathologische Gradierung ist von prognostischer Bedeutung. Sie erfolgt auf Grund des Systems von Bloom, Richards und Scarff, modifiziert nach Ellis (sogenannter BRE-Score).
4.2.3 Molekulare Subtypen
Auf der Basis von Genexpressionsprofilen können biologisch distinkte Subtypen des Mammakarzinoms unterschieden werden. Im St. Gallen Konsensus 2011 wird die Identifikation dieser Subtypen mittels histochemischer Surrogatparameter als Basis für die Entscheidung zur adjuvante systemischen Therapie empfohlen, siehe Tabelle 4.
Molekularer Subtyp | Subgruppe | Definition | Anmerkungen |
Luminal A |
| ||
Luminal B | HER2 negativ |
| |
HER2 positiv |
| ||
HER-2 enriched |
| ||
Basal like |
| weitgehende Überlappung mit dem triple (dreifach) negativen Karzinom |
*nach [10]
5 Therapie
Therapieoptionen beim lokal begrenzten Mammakarzinom umfassen die Operation, die Bestrahlung und die medikamentöse Tumortherapie [7, 8, 9, 10]. Ein Therapie - Algorithmus ist in Abbildung 1 dargestellt.
BET, Brusterhaltende Therapie; BSC, ‚Best Supportive Care‘
Grundlage der Behandlungsempfehlung an die Patientin ist die qualitätsgesicherte Erhebung der relevanten Risikofaktoren, siehe Abbildung 3.
5.1 Lokal begrenzte Stadien
Lokal begrenzte Karzinome umfassen die Stadien<IIB.
5.1.1 Operation
5.1.1.1 Brust
Ziel der Therapie ist die Exstirpation des Tumors mit einem tumorfreien Resektionsrand von 1 mm und mehr (R0). Die brusterhaltende Therapie (BET) mit adjuvanter Bestrahlung ist der modifizierten radikalen Mastektomie (MRM) bezüglich des Überlebens gleichwertig [11].
Indikationen für eine brusterhaltende Therapie (BET) sind
invasives Karzinom mit günstiger Relation von Tumorgröße zu Brustvolumen
invasives Karzinom mit intraduktaler Begleitkomponente, wenn eine R0 Situation erreicht wird
Indikationen für eine modifizierte radikale Mastektomie (MRM) sind
Multizentrizität
diffuse, ausgedehnte Kalzifikation vom malignen Typ
inkomplette Entfernung des Tumors bei BET (inkl. intraduktaler Komponente), auch nach Nachresektion
inflammatorisches Mammakarzinom
voraussichtlich nicht zufrieden stellendes kosmetisches Ergebnis bei BET
klinische Kontraindikationen zur Nachbestrahlung nach BET
Wunsch der Patientin
Plastisch rekonstruktive Eingriffe können im Rahmen des Primäreingriffs oder zum einem späteren Zeitpunkt durchgeführt werden.
5.1.1.2 Axilla
Standard zur Evaluation axillärer Lymphknoten ist die Sentinel-Lymph-Node Technik (SLNE) mit gezielter Entfernung und Untersuchung von ein bis drei Lymphknoten [12]. Die SLNE ist der Axilladissektion gleichwertig hinsichtlich der lokalen Kontrolle, aber mit einer geringeren Morbidität belastet. Bei positivem Sentinel-Lymphknoten galt bisher eine Axilladissektion mit Entfernung von mindestens 10 Lymphknoten aus Level I und II als indiziert. Aktuell wird dieses Konzept hinterfragt. Hintergrund ist eine Anfang 2011 publizierte Studie, bei der Patientinnen mit positivem Sentinel-Lymphknoten unter definierten Kriterien für oder gegen eine Axilladissektion randomisiert wurden. Nach einer medianen Beobachtungszeit von 6,3 Jahren waren die onkologischen Ergebnisse in beiden Armen, siehe Studienergebnisse Mammakarzinom . Die Patientinnen erfüllten folgende Kriterien:
Tumorstadium T1 oder T2
Sentinel Lymphknoten positiv
präoperativ cN0, d. h. kein klinischer Anhalt für einen Befall der Axilla
brusterhaltende Operation
intraoperativ kein Hinweis auf Adhärenz der Lymphknoten
postoperative Bestrahlung der Brust mit tangentialen Feldern
adäquate adjuvante medikamentöse Tumortherapie
Standard für die Untersuchung der Sentinel-Lymphknoten ist die Histologie. Der Nachweis isolierter Tumorzellen oder das Vorliegen von Mikro-Metastasen bis zu 2mm in einem einzigen Lymphknoten haben keine prognostische Relevanz. Sie beeinflussen das therapeutische Vorgehen nicht und stellen keine Indikation für eine Axilladissektion dar.
Bei primärer (neoadjuvanter) systemischer Therapie ist das Konzept der Sentinel-Lymphknoten-Biopsie umstritten. Auf der einen Seite steht die Chance einer Stadien-adjustierten Verringerung positiver Lymphknoten mit Reduktion der Notwendigkeit einer Axiiladissektion. Auf der anderen Seite steht das Risiko falsch negativer Befunde. Eine Alternative ist die prätherapeutische Sentinel-Lymphknoten-Biopsie. Die Ergebnisse großer prospektiver Studien stehen aus.
Ob eine Resektion des Primärtumors und ein operatives axilläres Staging bei Patientinnen im Stadium M1 die Prognose verbessert, ist unsicher und kein Standardvorgehen.
5.1.2 Bestrahlung
Die postoperative Bestrahlung halbiert die lokoregionäre Rezidivrate [13] und kann zur Verlängerung der Überlebenszeit beitragen. Es wird empfohlen, die Bestrahlung 4-6 Wochen nach Operation oder nach Abschluss einer adjuvanten Chemotherapie zu beginnen.
5.1.2.1 Brust / Brustwand
Nach brusterhaltender Operation (BET) ist eine adjuvante Bestrahlung der betroffenen Brust indiziert. Sie senkt das lokale Rezidivrisiko um zwei Drittel (HR 0,33), siehe Studienergebnisse Mammakarzinom Das Zielvolumen schließt die gesamte verbliebene Brust und die angrenzende Thoraxwand ein. Das optimale Bestrahlungsschema wird aktuell diskutiert [14,15]. Standard ist die konventionelle Fraktionierung mit der Applikation von 50 Gy in 25 Sitzungen über 5 Wochen. Bei der hypofraktionierten Bestrahlung werden bei Nachbeobachtungszeiten von 6-10 Jahren ähnliche Langzeitresultate beobachtet nach Applikation von 40 - 42,5 Gy in 15-16 Fraktionen über 3 Wochen.
Eine zusätzliche Boost-Bestrahlung des Tumorbettes mit 16 Gy führt zu einer weiteren, signifikanten Senkung der Lokalrezidivrate (HR 0,59).
Eine vergleichbar niedrige Lokalrezidivrate wird bei Patientinnen mit frühem Mammakarzinom auch durch eine intraoperative Teilbestrahlung der Brust erreicht, siehe Studienergebnisse Mammakarzinom.Vorteil ist eine Reduktion der Strahlenbelastung. Da Langzeitergebnisse noch ausstehen, ist die Teilbestrahlung der Brust bisher keine Standardtherapie.
Nach Mastektomie ist eine Bestrahlung der Brustwand zur Senkung der Lokalrezidivrate und zur Verbesserung der brustkrebsspezifischen Mortalität bei Patientinnen mit positiven Lymphknoten, insbesondere >3 positiven Lymphknoten, indiziert. Auch bei dem Vorliegen weiterer Risikofaktoren (Alter <40 Jahre, Lymph- oder Hämangiosis, pT2 >3 cm, Infiltration der Pektoralisfaszie, R1 / R2 Situation) ist der Nutzen einer Bestrahlung plausibel [7, 8].
5.1.2.2 Regionale Lymphabflusswege
In der derzeit gültigen deutschen S3 Leitlinie wird eine Bestrahlung empfohlen bei Resttumor der Axilla, und wenn bei eindeutigem, klinischem Befall keine Axilladissektion durchgeführt wurde. Die aktuellen Daten legen nahe, dass bei positivem Sentinel-Lymphknoten nach brusterhaltender Resektion eine konventionelle tangentiale Ganzbrustbestrahlung ausreichend ist, sieheKapitel 5. 1. 1. 2.
Eine Bestrahlung der supra- und infraklavikulären Lymphabflusswege wird empfohlen bei>4 positiven axillären Lymphknoten, bei Befall des Level III der Axilla und bei anderen Indikationen zur Bestrahlung der Axilla.
Die Publikation der Ergebnisse randomisierter Studien zum Einfluss der Bestrahlung regionaler Lymphabflusswege bei Patientinnen im Stadium II und III nach brusterhaltender Operation und Brustbestrahlung stehen aus, siehe Studienergebnisse Mammakarzinom .
5.1.3 Adjuvante endokrine Therapie
Etwa 80 % der invasiv duktalen Mammakarzinome exprimieren Östrogenrezeptoren (ER) oder Progesteronrezeptoren (PgR). Kriterium für ein endokrin sensitives Karzinom ist der immunhistochemische Nachweis von>1% ER positiver Tumorzellen.
Die Bestimmung soll nach den Empfehlungen der Fachgesellschaften erfolgen [7, 8, 16]. Bei Patientinnen mit Östrogenrezeptor- und/oder Progesteronrezeptor - positivem Mammakarzinom ist eine endokrine Therapie indiziert. Der Therapie - Algorithmus ist in Abbildung 2 dargestellt.
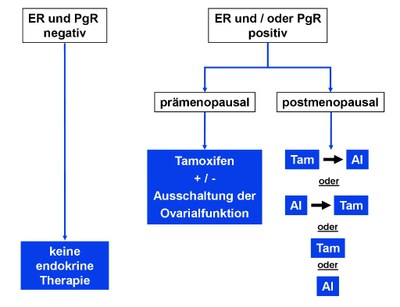
AI - Aromataseimhibitor, ER - Östrogenrezeptor; Tam - Tamoxifen; der Pfeil steht für Sequenz;
steht für Sequenz;
Beim Einsatz von Tamoxifen soll die endokrine Behandlung erst nach Abschluss der Chemotherapie begonnen werden.
5.1.3.1 Prämenopausal
Der Menopausenstatus wird durch die Menstruationsanamnese sowie die Laboruntersuchung von FSH und Östradiol (E2) bestimmt. Basis der endokrinen Therapie ist Tamoxifen, s. Abbildung 2. Die Frage, ob zusätzlich die Ovarialfunktion ausgeschaltet werden muss, ist nicht eindeutig geklärt. Für die Ausschaltung der Ovarialfunktion sind drei Methoden gleichwertig [7, 8, 9, 17]:
GnRH Analoga (GnRHa)
Ovarektomie
Radiomenolyse
Aromataseinhibitoren sind nicht indiziert. Die Kombination von GnRH Analoga mit Anastrozol statt mit Tamoxifen war statistisch gleichwertig in Bezug auf krankheitsfreie Überleben, hatte jedoch potenziell einen negativen Effekt auf die Gesamtüberlebensrate der Patientinnen, siehe Studienergebnisse Mammakarzinom . Prämenopausale Frauen, die in den 5 Jahren Tamoxifen postmenopausal werden, können von einer erweiterten adjuvanten Therapie mit einem Aromataseinhibitor profitieren.
5.1.3.2 Postmenopausal
Für die adjuvante endokrine Systemtherapie der postmenopausalen Patientin stehen Tamoxifen und Aromataseinhibitoren zur Verfügung, s. Abbildung 2. Tamoxifen halbiert die Rezidivwahrscheinlichkeit (relatives Risiko 0,53) und führt zu einer Verlängerung der Gesamtüberlebenszeit, verglichen mit Patientinnen ohne adjuvante endokrine Systemtherapie [18]. Aromataseinhibitoren senken das Rezidivrisiko um weitere 3% [19]. Für den Zeitpunkt des Einsatzes der Aromataseinhibitoren gibt es mehrere Optionen:
Sequenz (Switch) nach 2 - 3 jähriger Tamoxifen - Therapie
Sequenz (Switch) nach 5 jähriger Tamoxifen Therapie
Monotherapie (upfront)
Bei Einsatz als Ersttherapie (upfront) führen Aromatase-Inhibitoren in den ersten beiden Jahren nach Therapiebeginn zu einer signifikanten Senkung des Rezidivrisikos und in der Zulassungsstudie zu Letrozol zu einer Senkung der Mortalität. In den Switch-Studien nach Tamoxifen senken sie die Mammakarzinom-spezifische Mortalität [19], siehe Studienergebnisse Mammakarzinom .
5.1.3.3 Dauer der endokrinen Therapie
Der Standard für die Dauer der adjuvanten endokrinen Therapie orientierte sich bisher an 5 Jahren Tamoxifen. Eine Verlängerung der endokrinen Therapie mit Aromataseinhibitoren senkt das Rezidivrisiko. In der aktuell vorgestellten ATLAS Studie führte die adjuvante Therapie mit Tamoxifen über 10 verglichen mit 5 Jahren zu einer signifikantenn Senkung des Rezidivrisikos, der Brustkrebs-spezifischen und der Gesamtmortalität, siehe Studienergebnisse Mammakarzinom .
5.1.3.4 Substanzen
GnRH (LHRH) - Analoga
GnRH Analoga blockieren die Produktion von weiblichen und männlichen Sexualhormonen auf der Regulationsebene. Beim Mammakarzinom sind sie wirksam in der adjuvanten und in der palliativen Therapie. Häufige, subjektiv belastende Nebenwirkungen bei der Frau sind Schwitzen, trockene Vaginalschleimhaut, Veränderung der Libido und Stimmungsschwankungen. GnRH Analoga werden subkutan oder intramuskulär als Implantat oder flüssiges Depot appliziert.
Tamoxifen
Tamoxifen ist ein selektiver Östrogenrezeptor-Modulator. Es wird im Körper über den Cytochrom P450 Weg zum wirksamen Metaboliten umgewandelt. Die Bedeutung des CYP2D6 Polymorphismus für die klinische Wirksamkeit von Tamoxifen wird kontrovers diskutiert. Beim Mammakarzinom ist Tamoxifen wirksam in der Prävention, in der adjuvanten Situation zur Rezidivpropylaxe und palliativ. Häufige, subjektiv belastende Nebenwirkungen sind leichte Übelkeit, Flüssigkeitsretention und Hitzewallungen. Kritische, schwere Nebenwirkungen sind venöse Thrombembolien, Veränderung der Endometriumschleimhaut bis zur Entstehung eines Endometriumkarzinom und Reduktion der Knochendichte bei prämenopausalen Patientinnen. Bei postmenopausalen Patientinnen steigert Tamoxifen die Knochendichte.
Aromataseinhibitoren (AI)
Medikamente dieser Substanzgruppe verhindern die Synthese von Östrogenen aus Androgenen durch Blockade von Aromatase. Chemisch unterschieden werden steroidale AI (Exemestan) und nicht-steroidale AI (Anastrozol, Letrozol). Klinisch wirksam beim Mammakarzinom sind Aromataseinhibitoren in der Prävention und in der adjuvanten Therapie bei postmenopausalen Patientinnen, sowie palliativ. Häufige belastende Nebenwirkungen sind Arthralgien, Arthrose, Myalgien, Hitzewallungen und Verminderung der Knochendichte bis zur Osteoporose. Unter der Therapie wird eine regelmäßige Überwachung der Knochendichte sowie eine Prävention mit Vitamin D und Calcium empfohlen. Zoledronat und Denosumab können den Knochenabbau verhindern.
5.1.4 Adjuvante Chemotherapie
Adjuvante Chemotherapie senkt das Rezidivrisiko [20]. Der individuelle Nutzen ist abhängig von biologischen Charakteristika des Tumors, dem Tumorstadium, von Art und Intensität der Chemotherapie und von der Komorbidität.
5.1.4.1 Adjuvante Chemotherapie - Indikation
In Abbildung 3 sind die Risikofaktoren in drei Kategorien geordnet, je nach ihrer Wertigkeit für den Nutzen einer adjuvanten Chemotherapie, gegen den Nutzen einer Chemotherapie oder als Faktoren unklarer Signifikanz. Die zusammenfassende Bewertung ist Grundlage der Behandlungsempfehlung.
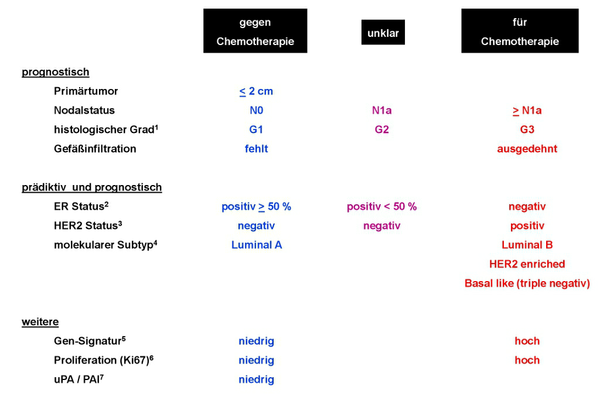
1G - Grading;2ER - Östrogenrezeptor;3HER2 - Human Epidermal growth factor Receptor; HER2 negativ - keine HER2 Überexpression / keine HER2 Genamplifikation; HER2 positiv - HER2 Überexpression und / oder HER2 Genamplifikation;4molekular Subtypen - zur Definition siehe Kapitel 4.2.3.;5Gen-Signatur - Auswertung der Transkription Prognose-relevanter Gene, siehe Text Kapitel 5.1.4.1.;6Proliferation - konventionelle Methoden sind der Ki67-Labelling Index und die Auszählung der Mitoserate, siehe TextKapitel 5.1.4.1.;7uPA / PAI-1 - Urokinase-Type Plasminogen Activator und Plasminogen Activator Inhibitor Type 1, siehe TextKapitel 5.1.4.1.;
Neu ist die Aufnahme von Gen-Signaturen in den Algorithmus. Das Ergebnis dieser molekularbiologischen Analyse am Tumormaterial wird in einem Risiko-Score ausgedrückt. Retrospektive Studien deuten darauf hin, dass Patientinnen mit einem ER positiven Mammakarzinom und einem niedrigen Risikoscore nicht oder nur in geringem Ausmaß von adjuvanter Chemotherapie profitieren. Die Ergebnisse großer prospektiver Studien mit den kommerziell bereits erhältlichen Tests stehen aus.
Die Proliferationsrate ist ein wichtiger prognostischer Faktor. Allerdings weist die dafür eingesetzte mikroskopische Zählung Ki67-positiver Zellen eine hohe Schwankungsbreite breit. Ein Schwellenwert, der die Entscheidung für oder gegen eine adjuvante Chemotherapie prospektiv unterstützt, ist bisher nicht validiert.
Die Bedeutung der Aktivität von Urokinase-Type Plasminogen Activator und Plasminogen Activator Inhibitor Type 1 (uPA/PAI-1) wurde prospektiv validiert. Sie wird in Deutschland angewandt, international ist sie auch aufgrund der fehlenden Verfügbarkeit von frischem Tumorgewebe nicht als Standard anerkannt.
Die Chemotherapie ist indiziert bei Patientinnen mit triple negativem Mammakarzinom, d. h. fehlender Expression von Hormonrezeptoren und von HER2. Davon ausgenommen sind seltene Formen wie das typische medulläre Mammakarzinom bei Patientinnen ohne BRCA Mutation, das apokrine und das adenoidzystische Mammakarzinom. Diese sind zwar triple negativ, haben aber kein erhöhtes Risiko für eine Metastasierung. Bei Patientinnen mit triple negativem Mammakarzinom pT1a pN0 ist der Nutzen einer adjuvanten Chemotherapie nicht belegt.
Die adjuvante Chemotherapie ist auch indiziert beim HER2-positiven Karzinom, da die Studien zum Nachweis der Effektivität von Trastuzumab nur in dieser Kombination durchgeführt wurden.
5.1.4.2 Substanzen
In der adjuvanten Chemotherapie des Mammakarzinoms werden mindestens zwei, häufiger drei Zytostatika kombiniert. Diese können simultan oder sequentiell appliziert werden. Evaluiert ist eine Vielzahl von Kombinationen und Applikationsschemata. Die definitive, standardisierte Zuordnung eines bestimmten Chemotherapie - Regimes zu einer spezifischen Risikokonstellation gibt es z. Zt. nicht [7, 8, 9]. Die publizierten Ergebnisse randomisierter klinischer Studien sind in Mammakarzinom Studienergebnisse zusammengestellt und zeigen:
Anthrazykline
Anthrazylin - haltige Kombinationen sind effektiver als CMF. Ausnahme ist die Äquieffektivität von 4 x AC und 6 x CMF im dreiwöchentlichen Rhythmus bei Patientinnen mit ER-negativem Mammakarzinom.
Die berechnete Dosierung von Doxorubicin sollte>20 mg / m2/ Woche und von Epirubicin>30 mg / m2/ Woche betragen. (Anthrazykline werden in zwei- oder dreiwöchentlichen Intervallen gegeben; zur Vergleichbarkeit wird die berechnete Dosis pro Woche angegeben.)
Bei Kontraindikationen gegen Anthrazykline ist CMF effektiver als keine Chemotherapie. Bei Patienten >65 Jahre ist CMF wirksamer als eine Monotherapie mit Capecitabin.
Eine weitere Alternative, besonders bei Kontraindikationen gegen Anthrazykline, kann die Kombination von Docetaxel und Cyclophosphamid sein.
Taxane
Kombinationen von Taxanen und Anthrazyklinen - gleichzeitig oder sequenziell appliziert - sind effektiver als nur Anthrazyklin-haltige Schemata bei Patientinnen mit erhöhtem Rezidivrisiko. Der Effekt ist unabhängig von Alter, Menopausenstatus, Zahl der betroffenen Lymphknoten und Hormonrezeptorstatus.
Die sequenzielle Applikation von 4 x Docetaxel nach 4 x Doxorubicin / Cyclophosphamid ist der gleichzeitigen Gabe der drei Substanzen im Hinblick auf das krankheitsfreie Überleben und das Gesamtüberleben gleichwertig, sieheStudienergebnisse Mammakarzinom.Die gleichzeitige Gabe ist mit einem erhöhten Infektionsrisiko assoziiert und erfordert höhere kumulative Dosen von Anthrazyklinen und Taxanen.
Docetaxel und Paclitaxel haben sind grundsätzlich als gleichwertig erwiesen. In der sequenziellen Therapie nach Anthrazyklin waren die wöchentliche Gabe von Paclitaxel oder die dreiwöchentliche Gabe von Docetaxel wirksamer als die dreiwöchentliche Gabe von Paclitaxel.
Die wöchentliche statt der dreiwöchentlichen Applikation ändert auch das Nebenwirkungsspektrum.
Dosisdichte Therapie / Dosiseskalation / Hochdosistherapie mit autologer Stammzelltransplantation
Eskalation der Zytostatikadosis und Verkürzung der Therapieintervalle kann das krankheitsfreie Überleben vor allem bei Patientinnen mit ER-negativem Mammakarzinom verbessern und führt in einigen Studien zu einer Verlängerung der Überlebenszeit, siehe Studienergebnisse Mammakarzinom.
Die Intensivierung der Chemotherapie mit supportiver autologer Stammzelltransplantation führt nicht zu einer Verbesserung der Gesamtüberlebensrate und wird in der adjuvanten Therapie nicht empfohlen [21].
5.1.4.3 Adjuvante chemoendokrine oder endokrine Therapie?
Die Frage, bei welchen Patientinnen im Falle einer HR-Positivität eine alleinige endokrine Therapie einer chemoendokriner Sequenztherapie als gleichwertig anzusehen ist, ist nicht endgültig geklärt [22]. siehe Studienergebnisse Mammakarzinom . Aus den vorliegenden Daten lassen sich folgende Anhaltspunkte für eine Therapieentscheidung ableiten:
Prämenopausal
Die adjuvante endokrine Therapie mit Goserelin und Tamoxifen erzielt bei prämenopausalen Patientinnen mit ER-positivem Mammakarzinom (>10% ER-positive Zellen in der Immunhistochemie) und Befall von höchstens 3 axillären Lymphknoten krankheitsfreie Überlebensraten von >90 % nach 5 Jahren, siehe Studienergebnisse Mammakarzinom .
In retrospektiven Subgruppenanalysen ist die chemoendokrine Therapie einer rein endokrinen Therapie überlegen bei einer ER Expression <90% der Zellen, bei fehlender PgR Expression und einem Alter <40 Jahre.
Beim HER2 positiven Mammakarzinom ist die chemoendokrine Sequenztherapie Standard, in Kombination mit einer anti-HER2 Therapie (siehe unten).
Bei Kinderwunsch sollte die Patientin vor Beginn einer eventuellen Chemotherapie ausführlich über fertilitätserhaltende Maßnahmen informiert werden, siehe Onkopedia Leitlinie Heranwachsende und junge Erwachsene (AYA) .
Die alleinige antihormonelle Therapie ist eine Option bei Kontraindikationen gegen Chemotherapie.
Postmenopausal
Parameter für die Therapieentscheidung sind Allgemeinzustand, Komorbidität und Rezidivrisiko, nicht das nummerische Alter.
Der Überlebenszeit-Vorteil einer chemoendokrinen Sequenztherapie zeigt sich nur bei Patientinnen mit einer mutmaßlichen Lebenserwartung>10 Jahren.
Patientinnen mit Mammakarzinomen vom Typ Luminal A profitieren wahrscheinlich nicht von einer adjuvanten Chemotherapie.
5.1.5 Adjuvante anti - HER2 Therapie
Etwa 20 % der invasiv duktalen Mammakarzinome exprimieren den Human - Epidermal growth factor Receptor 2 (HER2). Die Analyse des HER2 Status soll mittels eines genauen und validierten Verfahrens durchgeführt werden. HER2 Positivität ist definiert durch:
Immunhistochemie: Score 3+
Fluoreszenz - in - situ - Hybridisierung (FISH): HER2/Zentromer 17 - Quotient >2
Chromogene - in - situ - Hybridisierung (CISH): >6 HER2 Signale / Nukleus
Als Medikament steht der monoklonale Antikörper Trastuzumab zur Verfügung. Die adjuvante Therapie mit Trastuzumab senkt das Rezidivrisiko im Vergleich zu ausschließlicher Chemotherapie und verlängert die Überlebenszeit [7, 8, 9, 10], siehe Studienergebnisse Mammakarzinom .
Patientinnen mit HER2-Positivität sollen eine adjuvante Therapie mit Trastuzumab über ein Jahr erhalten. Ausnahme können Patientinnen mit nodal negativem Mammakarzinom und einer Tumorgröße <5 mm sein, für die keine ausreichenden Daten vorliegen. Die großen randomisierten Studien zur Wirksamkeit von Trastuzumab wurden ausschließlich mit Chemotherapie durchgeführt, entweder kombiniert oder sequenziell. Trastuzumab wird bevorzugt simultan zu Taxanen und sequentiell nach Anthrazyklinen gegeben. Ob Subgruppen von Patientinnen mit hoher endokriner Sensitivität auch von einer ausschließlichen Kombination endokriner Therapie mit Trastuzumab profitieren, ist nicht geklärt.
5.1.6 Adjuvante Therapie mit Bisphosphonaten
Bisphosphonate und RANKL Antikörper reduzieren das Osteoporose - Risiko und haben potenziell auch klinisch relevante, antineoplastische Eigenschaften. Die Ergebnisse randomisierter Studien sind uneinheitlich. Nachdem einige Studien bei postmenopausalen Patientinnen einen positiven Einfluss auf das krankheitsfreie Überleben gezeigt hatten, fand sich in der aktuell publizierten, umfangreichsten randomisierten Studie im Gesamtkollektiv prä- und postmenopausaler Patientinnen kein signifikanter Unterschied zugunsten von Zoledronat. Demgegenüber steht eine Verbesserung des krankheitsfreien und des Gesamtüberlebens durch Zoledronat in einer Studie bei prämenopausalen Patientinnen unter gleichzeitiger adjuvanter endokriner Therapie, siehe Studienergebnisse Mammakarzinom . Eine Indikation zum Einsatz von Bisphosphonaten oder des RANKL-Antikörpers Denosumab ist die Osteoporose unter adjuvanter Therapie mit Aromataseinhibitoren.
5.2 Lokal fortgeschrittene Stadien
Lokal fortgeschrittene Karzinome umfassen die Stadien IIIA und B.
5.2.1 Primäre (neoadjuvante, präoperative) systemische Therapie
Eine primäre (neoadjuvante, präoperative) systemische Therapie ist in folgenden Situationen indiziert:
lokal fortgeschrittenes Mammakarzinom
primär inoperables Mammakarzinom
inflammatorisches Mammakarzinom
Reduktion der Grösse des Primärtumors mit der Chance zur Vermeidung einer Mastektomie
Alternative zu einer postoperativen adjuvante Therapie, die aufgrund der klinischen, bildgebenden und bioptischen Resultate indiziert wäre
HER2 positives Karzinom
triple negatives Karzinom
klinische Studie
In randomisierten Studien sind krankheitsfreie und Gesamt - Überlebenszeit nach primärer oder adjuvanter systemischer Therapie gleich [23]. Bei Patientinnen mit fehlender Hormonsensitivität können pathohistologische Komplettremissionen (pCR) des Primärtumors von 40% erzielt werden. Patientinnen, die nicht auf eine primäre systemische Chemotherapie ansprechen, haben eine ungünstige Prognose. Die eingesetzten Schemata entsprechen denen der adjuvanten Therapie mit Applikation von Anthrazyklinen und Taxanen über eine Behandlungsdauer von mindestens 18 Wochen.
Bei Patientinnen mit HER2 überexprimierenden bzw. genamplifizierten Mammakarzinom ist zusätzlich die Gabe von Trastuzumab indiziert.
Die primäre endokrine Therapie stellt eine Option für postmenopausale Patientinnen mit ER positivem Tumor dar, bei denen Operation oder Chemotherapie kontraindiziert sind oder abgelehnt werden.
Unter einer primären (neoadjuvanten) Therapie sind engmaschige Kontrollen einschl. bildgebender Untersuchung des Tumors erforderlich. Ggfs. muss bei kleinen Tumoren eine Clipmarkierung erfolgen, um auch bei pCR das Tumorbett sicher operativ entfernen zu können. Primäre Option bei einer Progression ist die frühzeitige Operation.
5.2.2 Multimodale Therapie
Die primäre systemische Chemotherapie ist Teil eines multimodalen Behandlungskonzepts und wird fortgesetzt mit Operation, Bestrahlung sowie medikamentöser Tumortherapie entsprechend den Indikationen beim lokal begrenzten Mammakarzinom.
5.3 Lokoregionäres Rezidiv
Die Inzidenz lokoregionärer Rezidive liegt bei 5-10% innerhalb von 10 Jahren nach brusterhaltender Operation (BET) und Bestrahlung, etwas niedriger nach Mastektomie. Bei etwa 90% entstehen sie in der Brust (In-Brust-Rezidiv), seltener an der Thoraxwand oder in der Axilla. Der Therapieanspruch beim lokoregionären Rezidiv ist kurativ, sofern keine simultanen Fernmetastasen entdeckt werden, s. Abbildung 4. Die prognostischen Faktoren entsprechen denen der Primärtumore. Ein zusätzlicher negativer Faktor ist ein kurzes Intervall zwischen Erstdiagnose und Rezidiv. Primäres Ziel ist die lokale Kontrolle durch Operation und / oder Bestrahlung. Es gibt nur wenige Studien zum Wert einer medikamentösen Tumortherapie in der Sekundärprophylaxe. Die adjuvante Therapie mit Tamoxifen bei Patientinnen mit ER positivem Karzinom und einem Intervall >12 Monate nach Ersttherapie verhindert vor allem das Auftreten weiterer Lokalrezidive, sieheStudienergebnisse Mammakarzinom.Eine adjuvante Chemotherapie führt zu einer signifikanten Verbesserung des progressionsfreien und des Gesamtüberlebens.
Mögliche Ansätze für eine medikamentöse Tumortherapie sind
endokrine Therapie: Wechsel von Tamoxifen auf Aromataseinhibitoren bzw. vice versa
Chemotherapie: empfohlen; die Wahl der Medikamente ist davon abhängig, ob bei Erstmanifestation eine adjuvante Chemotherapie durchgeführt wurde und ob die neueren Substanzen (Anthrazykline, Taxane) eingesetzt wurden.
5.4 Fernmetastasen
Trotz effektiver Primärtherapie und Fortschritten in der adjuvanten Behandlung treten bei etwa 20 % der Patientinnen Fernmetastasen auf. In dieser Situation ist die Therapie in der Regel palliativ.
Mit einer überdurchschnittlichen Lebenserwartung sind assoziiert:
guter AZ
ausschließlicher Befall von Skelett, Lymphknoten, Haut
ER Positivität
keine HER2 Überexpression / keine HER2 Genamplifikation
rezidivfreies Intervall >2 Jahre
keine adjuvante Therapie
keine Vortherapie im metastasierten Stadium
Palliative Therapie beinhaltet die Behandlung körperlicher und psychischer Beschwerden. Sie erfolgt interdisziplinär. Die Diagnostik erfolgt Symptom- und Therapie-orientiert, s. Tabelle 2. Wenn möglich, sollte eine Biopsie zur histologischen Bestätigung des Rezidivs, zur aktuellen Analyse von ER- und HER2-Status, und zum Ausschluss eines Zweitmalignoms gewonnen werden.
Die kausale Therapie wird von der Biologie der Erkrankung bestimmt. Ein Algorithmus ist in Abbildung 4 dargestellt.
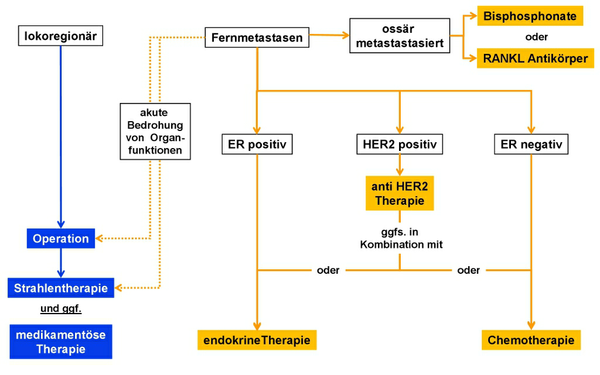
1ER - Östrogenrezeptor;2HER2 - Human Epidermal growth factor Receptor; HER2 positiv - HER2 Überexpression / HER2 Genamplifikation
Neben der kausalen, systemischen Therapie kommen auch Symptom-orientierte Verfahren einen hohen Stellenwert.
Bei Patientinnen mit Befall eines einzigen Organs (z. B. Leber, Lunge, Gehirn, Sternum) können durch Lokaltherapie (Operation, Bestrahlung o.ä.) mit / oder ohne adjuvanter medikamentöser Therapie überdurchschnittlich gute Fünfjahres-Überlebensraten erreicht werden. Randomisierte Studien zum langfristigen, onkologischen Wert der Lokaltherapie stehen aus. Es wird empfohlen, die Behandlung bei diesen Patientinnen zunächst medikamentös zu beginnen, bevor zusätzlich lokale Maßnahmen eingesetzt werden.
Eine kleine Gruppe von Patientinnen präsentiert sich mit primär metastasiertem Krankheitsbild. Im Vordergrund steht bei diesen Patientinnen die systemische Therapie. Retrospektive Analysen sprechen für einen zusätzlichen Gewinn durch Resektion des Primärtumors. Indikation und optimaler Zeitpunkt sind aktuell Gegenstand prospektiver Untersuchungen, sieheKapitel 9. Aktive Studien.
5.4.1 Palliative endokrine Therapie
Bei Patientinnen mit ER positivem Mammakarzinom steht die endokrine Therapie an erster Stelle [24], siehe Abbildung 5. Eine Ausnahme ist vitale Bedrohung oder Bedrohung von Organfunktionen durch die Metastasierung. Die Remissionsraten der endokrinen Therapie liegen bei etwa 30-40%, siehe Studienergebnisse Mammakarzinom . Im Vergleich zur Chemotherapie sind die Nebenwirkungen geringer, die Remissionsdauer ist länger. Bei HER2 positivem Karzinom wird die endokrine Therapie in Kombination mit einer anti-HER2 Therapie durchgeführt. Die palliative endokrine Therapie wird bis zum Progress fortgeführt.
Das Auftreten unerwünschter Wirkungen wird durch Anamnese, klinische Untersuchung, Laboranalysen und ggfs. bildgebende Diagnostik etwa alle 4 Wochen überwacht. Das Ansprechen auf die Systemtherapie wird alle 2 bis 3 Monate mittels klinischer Untersuchung, Bestimmung geeigneter Laborparameter und gezielter, bildgebender Diagnostik kontrolliert.
5.4.1.1 Prämenopausal
Therapie der Wahl bei der prämenopausalen Patientin ist die Ausschaltung der Ovarialfunktion (GnRH Analoga, Ovarektomie oder - selten - die Radiomenolyse), in Kombination mit Tamoxifen. Bei Progress unter laufender endokriner Therapie ist eine Änderung der eingesetzten Medikation erforderlich. Der Algorithmus für die palliative endokrine Therapie ist in Abbildung 5 dargestellt.
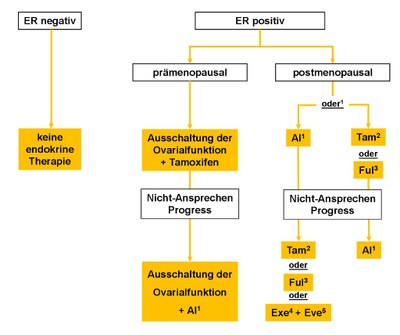
1AI - Aromataseinhibitor;2Tam - Tamoxifen;3Ful - Fulvestrant;4Exe - Exemestan;5Eve - Everolimus;
5.4.1.2 Postmenopausal
Therapie der Wahl bei der postmenopausalen Patientin sind steroidale oder nicht-steroidale Aromataseinhibitoren, s. Abbildung 5. Tamoxifen oder Toremifen sind die Alternativen. Allerdings wurden die Studien, welche die Überlegenheit der Aromataseinhibitoren zeigten, vor deren Einsatz in der adjuvanten Therapie durchgeführt. Bei Versagen dieser Medikamente wird die Zweit- bzw. Drittlinienbehandlung mit Fulvestrant empfohlen. Weitere Formen endokriner Therapie sind die Gabe von Gestagenen, Östrogenen, Androgenen oder der Wechsel zwischen steroidalem und nicht-steroidalem Aromataseinhibitor.
Nach Therapieversagen unter einem nicht-steroidalen Aromataseinhibitor führt die Kombination von Exemestan und Everolimus zu einer signifikanten Verlängerung der progressionsfreien Überlebenszeit..
5.4.1.3 Substanzen (in alphabetischer Reihenfolge)
Anastrozol
Anastrozol ist ein nicht-steroidaler Aromataseinhibitor (AI). Remissionsraten liegen bei 30% in der Erstlinien-, bei 10-15% in der Zweitlinientherapie. Häufige unerwünschte Wirkungen von Aromatase-Inhibitoren sind gastrointestinale Beschwerden, Hitzewallungen, Schmerzen, periphere Ödeme und allgemeine Schwäche. Besonders belastend sind Arthralgien, Arthrose, Myalgien und eine Verminderung der Knochendichte bis zur Osteoporose mit erhöhtem Frakturrisiko. Unter der Therapie wird eine regelmäßige Überwachung der Knochendichte sowie eine Prävention mit Vitamin D und Calcium empfohlen. Zoledronat und Denosumab können den Knochenabbau verhindern.
Exemestan
Exemestan ist ein steroidaler Aromataseinhibitor (AI). Häufige unerwünschte Wirkungen von Aromatase-Inhibitoren sind gastrointestinale Beschwerden, Hitzewallungen, Schmerzen, periphere Ödeme und allgemeine Schwäche. Besonders belastend sind Arthralgien, Arthrose, Myalgien und eine Verminderung der Knochendichte bis zur Osteoporose mit erhöhtem Frakturrisiko. Unter der Therapie wird eine regelmäßige Überwachung der Knochendichte sowie eine Prävention mit Vitamin D und Calcium empfohlen. Zoledronat und Denosumab können den Knochenabbau verhindern.
Fulvestrant
Fulvestrant ist ein Antiöstrogen, das mit hoher Affinität an den Östrogenrezeptor (ER) bindet und sowohl diesen Rezeptor als auch den Progesteronrezeptor herunterreguliert. In der Zweitlinientherapie nach Antiöstrogenen liegen die Remissionsraten bei 10%. Die Wirkung ist Dosis-abhängig, 500mg sind etwas effektiver als 250mg, siehe Studienergebnisse Mammakarzinom. Nebenwirkungen, die bei mehr als 5% der Patientinnen auftraten, waren allgemeine Schwäche, Übelkeit, Hitzewallungen, Schmerzen, periphere Ödeme und Schmerzen. Fulvestrant wird monatlich intramuskulär injiziert
Goserelin
Goserelin gehört zu den GnRH Analoga. Es blockt die Produktion von Sexualhormonen auf der Regulationsebene. In der palliativen Therapie bei prämenopausalen Patientinnen ist die Injektion von Goserelin eine der Methoden zur Ausschaltung der hormonellen Ovarialfunktion. Häufige, subjektiv belastende Nebenwirkungen sind Schwitzen, trockene Vaginalschleimhaut, Veränderung der Libido und Stimmungsschwankungen. GnRH Analoga werden subkutan oder intramuskulär als Implantat oder flüssiges Depot appliziert.
Letrozol
Letrozol ist ein nicht-steroidaler Aromataseinhibitor (AI). In der palliativen Erstlinientherapie werden Remissionsraten von 30%, in der Zweitlinientherapie von über 20% erzielt. Häufige unerwünschte Wirkungen von Aromatase-Inhibitoren sind gastrointestinale Beschwerden, Hitzewallungen, Schmerzen, periphere Ödeme und allgemeine Schwäche. Besonders belastend sind Arthralgien, Arthrose, Myalgien und eine Verminderung der Knochendichte bis zur Osteoporose mit erhöhtem Frakturrisiko. Unter der Therapie wird eine regelmäßige Überwachung der Knochendichte sowie eine Prävention mit Vitamin D und Calcium empfohlen. Zoledronat und Denosumab können den Knochenabbau verhindern.
Tamoxifen
Tamoxifen ist ein selektiver Östrogenrezeptor-Modulator. Es wird seit über 40 Jahren in der Therapie von Patienten mit metastasiertem Mammakarzinom eingesetzt. Häufige, subjektiv belastende Nebenwirkungen sind leichte Übelkeit, Rückenschmerzen, periphere Ödeme, Hitzewallungen und Gewichtszunahme. Kritische, schwere Nebenwirkungen sind venöse Thrombembolien und Veränderungen der Endometriumschleimhaut bis zur Entstehung eines Endometriumkarzinoms. Tamoxifen führt bei prämenopausalen Patientinnen zu einer Verminderung, bei postmenopausalen Patientinnen zu einer Steigerung der Knochendichte.
5.4.2 Palliative nicht - endokrine Systemtherapie
Chemotherapie ist effektiv beim metastasierten Mammakarzinom, aber mit mehr Nebenwirkungen als die endokrine Therapie belastet. Bei Abwägung von Nutzen und Risiko ist die Chemotherapie indiziert bei Patientinnen nach Versagen einer endokrinen Therapie und bei ER negativem Karzinom. Sie ist auch indiziert, wenn aufgrund einer fortgeschrittenen, Organ - gefährdenden Metastasierung oder aufgrund einer sehr hohen Progressionsdynamik schnell eine Remission erzielt werden soll, s. Abbildung 4. Bei HER2 positivem Karzinom wird die Chemotherapie in Kombination mit einer anti-HER2 Therapie durchgeführt.
Symptomlinderung und Remissionen können mit einer Vielzahl von Substanzen und Kombinationen erreicht werden. Die definitive, standardisierte Zuordnung eines bestimmten Chemotherapie - Regimes zu einer spezifischen Risikokonstellation gibt es nicht [25, 26].
Anthrazykline und Taxane sind die wirksamsten Einzelsubstanzen, siehe Studienergebnisse Mammakarzinom.Sie können die Überlebenszeit sowohl in der Mono- als auch in Kombinationstherapien verlängern, und sollten frühzeitig eingesetzt werden. Die Zahl sinnvoller Therapien ist neben der Chemosensitivität vom biologischen Subtyp des Tumors, der Verträglichkeit, der kumulativen Toxizität und von der Zahl der verfügbaren Substanzen abhängig.
Der Einsatz von Anthrazyklinen und Taxanen in der palliativen Therapie ist auch sinnvoll, wenn nach Anthrazyklin- und/oder Taxan-enthaltender adjuvanter Chemotherapie ein Rezidiv auftritt, besonders wenn das therapiefreie Intervall mindestens 12 Monate beträgt.
Biologische Tests für die Auswahl der optimalen Therapie, z. B. Gensignatur oder In-vitro Sensitivität, sind bisher nicht ausreichend prospektiv validiert und stellen ebenso wie das Monitoring mittels der Bestimmung zirkulierender Tumorzellen kein Standardverfahren dar.
Das Auftreten unerwünschter Wirkungen wird durch Anamnese, klinische Untersuchung, Laboranalysen und ggfs. bildgebende Diagnostik bei jedem Therapiezyklus überwacht. Das Ansprechen auf die Systemtherapie wird alle 2 bis 3 Monate mittels klinischer Untersuchung, Bestimmung geeigneter Laborparameter und gezielter, bildgebender Diagnostik kontrolliert. Bei Patientinnen mit ausgedehnter und / oder rasch progredienter Metastasierung und bei Patientinnen mit ausgeprägter lokaler Symptomatik können engmaschigere Kontrollen indiziert sein.
5.4.2.1 Mono - oder Kombinationstherapie
Die Kombinationstherapie, entweder von Substanzen der Chemotherapie oder mit Bevacizumab, führt zu höheren Remissionsraten und längerem progressionsfreiem Überleben. In einigen Studien konnte eine Verlängerung der Überlebenszeit gezeigt werden, vor allem in Studien ohne Crossover-Design. Die Kombinationstherapie ist mit stärkeren Nebenwirkungen belastet. Bei geringen Beschwerden und langsamem Tumorwachstum ist eine Monotherapie sinnvoll [27, 28, 29]. Bei hohem Remissionsdruck aufgrund stärkerer Beschwerden, fortgeschrittenen viszeralen Metastasen oder raschem Tumorwachstum sollte eine Kombinationstherapie durchgeführt werden. Eine Alternative zur Kombinationschemotherapie ist die sequenzielle Applikation von einzelnen Zytostatika. Ein Algorithmus für die palliative Chemotherapie ist in den Abbildungen 6 und 7 dargestellt, aufgeteilt nach Mono- und Kombinationstherapie.
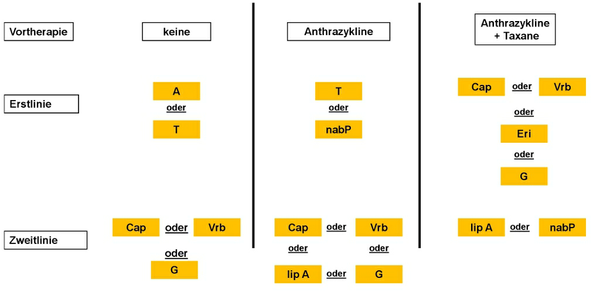
A - Anthrazyklin, Cap - Capecitabin, Eri - Eribulin, G - Gemcitabin, lip A - liposomales Doxorubicin, nabP - albumingebundenes Paclitaxel, Pac - Paclitaxel, T - Taxan, Vrb - Vinorelbin;
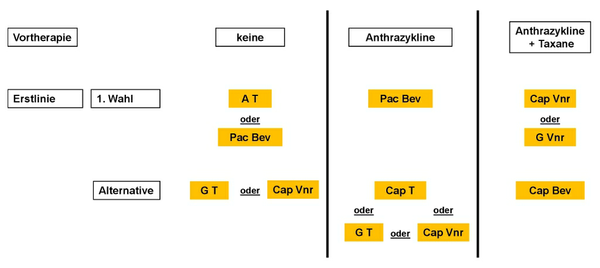
A - Anthrazyklin, Bev - Bevacizumab, Cap - Capecitabin, G - Gemcitabin, Pac - Paclitaxel, T - Taxan, Vrb - Vinorelbin;
5.4.2.2 Substanzen
Anthrazykline / Anthracene
Zu dieser Gruppe gehören Doxorubicin, Epirubicin, liposomales Doxorubicin und Mitoxantron. Sie gehören zu den wirksamsten Zytostatika beim metastasierten Mammakarzinom. Die mittleren Remissionsraten der Monotherapie bei nicht - vorbehandelten Patientinnen liegen zwischen 35 und 40%. Anthrazykline sind indiziert bei Patientinnen ohne Anthrazyklin-Vorbehandlung oder nach einem Intervall von mindestens 12 Monaten. Liposomales Doxorubicin ist eine Alternative bei Patientinnen mit Indikation für Anthrazykline und kardialer Komorbidität oder bei Erreichen der kumulativen Anthrazyklin - Höchstdosis. Schwere Nebenwirkungen (Grad 3/4) sind Alopezie, Mukositis und hämatologische Toxizität (Neutropenie, Thrombozytopenie, Anämie). Seltenere kritische Komplikation ist die linksventrikuläre Herzinsuffizienz aufgrund von Kardiomyopathie oder Rhythmusstörungen. Das Risiko kardialer Komplikation ist geringer bei Epirubicin oder liposomalem Doxorucibin. Übelkeit und Erbrechen können durch adäquate supportive Therapie verhindert werden.
Bendamustin
Die Wirkung dieser alkylierenden Substanz wurde in einer randomisierten Phase III Studie im Vergleich von B(endamustin)MF zu CMF nachgewiesen. Häufigere schwere Nebenwirkungen waren Mukositis und Leukozytopenie.
Bevacizumab
Bevacizumab ist ein monoklonaler, antiangiogenetisch wirksamer Antikörper. In Kombination mit Taxanen oder anderen Zytostatika (Anthrazykline, Capecitabin) führt er zu einer Steigerung der Remissionsraten sowie zu einer geringen aber statistisch signifikanten Verlängerung des progressionsfreien Überlebens, jeweils verglichen mit der Mono - Chemotherapie. Die Gesamtüberlebenszeit wird nicht verlängert, siehe Studienergebnisse Mammakarzinom . Schwere Nebenwirkungen (Grad 3/4), die bei mehr als 5% der Patienten in den Zulassungsstudien auftraten, waren Hypertonie und Proteinurie. Seltenere kritische Komplikationen sind thrombembolische Ereignisse und Perforationen im Gastrointestinaltrakt.
Capecitabin
Diese orale Substanz wird in der Leber zu Fluorouracil metabolisiert. Capecitabin ist in der Monotherapie wirksam mit Remissionsraten von 20 - 30%. Bessere Ergebnisse werden in Kombination mit Doxetaxel oder Bevacizumab erzielt. Capecitabin ist effektiv in der Behandlung des metastasierten HER2 positiven Mammakarzinoms nach Taxanen und Anthrazyklinen, auch in Kombination mit Lapatinib. Schwere Nebenwirkungen (Grad 3/4), die bei mehr als 5% der Patienten in den Zulassungsstudien auftraten, waren Stomatitis, Diarrhoe und Hand - Fuß - Syndrom.
Eribulin
Eribulin ist ein synthetisches Analogon von Halichondrin B, einer ursprünglich aus Meeresschwämmen isolierten, antineoplastisch wirkenden Substanz. Bei Patientinnen mit fortgeschrittenem Mammakarzinom führte es in der Drittlinientherapie nach Anthrazyklin- und Taxanbehandlung zu einer signifikanten Verlängerung der Überlebenszeit gegenüber einer Vergleichstherapie nach Wahl der behandelnden Ärzte. Die Remissionsraten lagen bei 12%. In einer aktuell vorgestellten randomisierten Studie war Eribulin einer festgelegten Monotherapie mit Capecitabin nicht überlegen, siehe Studienergebnisse Mammakarzinom . Schwere Nebenwirkungen (Grad 3/4), die bei mehr als 5% der Patienten in der Zulassungsstudie auftraten, waren: Neutropenie (45%), allgemeine Schwäche / Fatigue (9%) und Neuropathie (8%).
5-Fluorouracil
5-Fluorouracil (5FU) ist wirksam als Einzelsubstanz und in Kombinationen. 5FU kann entweder als Kurzinfusion oder als Dauerinfusion über 24 Stunden gegeben werden. Eine verstärkende Wirkung von Leukovorin wurde beim Mammakarzinom nicht nachgewiesen. Schwere Nebenwirkungen sind Diarrhoe und Stomatitis. Patienten mit funktionell relevanten Polymorphismen der Gene des 5-FU Abbaus haben ein erhöhtes Risiko für schwere Nebenwirkungen einschl. Neutropenie und neutropenisches Fieber.
Gemcitabin
In der Monotherapie werden Remissionsraten zwischen <10 und 20%, in der Kombinationstherapie mit Taxanen bis zu 60% erzielt. Nach Vorbehandlung mit Taxanen und Anthrazyklinen erreicht die Kombination mit Vinorelbin über 30% Remissionen. Schwere Nebenwirkung (Grad 3/4), die bei mehr als 5% der Patienten in den großen randomisierten Studien auftraten, war Neutropenie.
PARP Inhibitoren
Die Poly ([ADP]-Ribose) Polymerases (PARP) sind Enzyme der DNS - Reparatur und Ziele einer Gruppe neuer Medikamente. Präliminäre Wirksamkeitsdaten existieren beim triple negativen Mammakarzinom und bei Patienten mit BRCA Mutationen.
Platin
Platinderivate gehören zu den wirksamen Substanzen. Aktuelle Phase II- und eine Phase III- Studie zeigen Remissionsraten von über 50% in Kombinationstherapien mit Carboplatin mit Paclitaxel bei Patientinnen mit HER2 positivem bzw. beim triple negativen Karzinom. Schwere Nebenwirkungen (Grad 3/4) von Carboplatin, die bei mehr als 5% der Patienten auftreten, sind vor allem hämatologisch (Neutropenie, Thrombozytopenie, Anämie).
Taxane
Hierzu gehören Paclitaxel, Docetaxel und und Albumin - gebundenes Paclitaxel (nab Paclitaxel). Die mittleren Remissionsraten der Monotherapie bei nicht - vorbehandelten Patientinnen liegen zwischen 30 und 35%. In Kombination mit Anthrazyklinen werden höhere Remissionsraten von 55 - 60% und eine Verlängerung des progressionsfreien Überlebens erzielt. Die Studienergebnisse zu einer Verlängerung der Gesamtüberlebenszeit durch Taxan - haltige Kombinationen sind nicht einheitlich. Nach adjuvanter Vortherapie ist eine Retherapie möglich. Beim Paclitaxel ist die wöchentliche Applikation effektiver als die dreiwöchentliche Applikation. Schwere Nebenwirkungen (Grad 3/4) sind Alopezie, Infektionen, Nagelveränderungen, Stomatitis und Diarrhoe. Besonders belastend ist eine z. T. irreversible Polyneuropathie. Häufige Nebenwirkungen wie Übelkeit / Erbrechen und allergische Reaktionen können durch adäquate supportive Therapie verhindert werden.
Vinorelbin
Dieses Vinca - Alkaloid kann intravenös oder oral appliziert werden. Bei der Monotherapie wurden Remissionsraten von bis zu 25% erzielt. Es ist sowohl für die Mono- als auch für die Kombinationstherapie geeignet, auch mit Trastuzumab bei HER-2 Positivität. Schwere Nebenwirkungen (Grad 3/4), die bei mehr als 5% der Patienten auftreten, sind vor allem Neutropenie und Anämie.
5.4.3 Palliative anti-HER2 Therapie
Der monoklonale Antikörper Trastuzumab ist eine wirksame Substanz bei HER2 positiven Patientinnen mit Remissionsraten von 20%. In Kombination mit Anthrazyklinen, Taxanen, Capecitabin, Vinorelbin und Platinderivaten werden Remissionsraten von >50% mit einer signifikanten Verlängerung des progressionsfreien Überlebens gegenüber alleiniger Chemotherapie erreicht, siehe Studienergebnisse Mammakarzinom . Wegen eines erhöhten Kardiomyopathie - Risikos soll Trastuzumab nicht simultan mit Anthrazyklinen eingesetzt werden.
Lapatinib wird oral appliziert. Es ist wirksam bei Trastuzumab - vorbehandelten Patientinnen in Kombination mit Capecitabin. Trastuzumab und Lapatinib sind auch wirksam in Kombination mit Aromataseinhibitoren bei Patientinnen mit hormonsensitivem Mammakarzinom. Bei Progress unter Trastuzumab ist die Kombination von Lapitinib plus Trastuzumab wirksamer als eine Lapatinib Monotherapie.
Eine neue Substanz ist Pertuzumab, ein humanisierter Anti-HER2 Antikörper, der an ein anderes Epitop als Trastuzumab bindet. Die Hinzunahme von Pertuzumab zur Kombination Trastuzumab / Docetaxel führte zu Remissionsraten von 80% sowie einer signifikanten Verlängerung von progressionsfreier und Gesamtüberlebenszeit, siehe Studienergebnisse Mammakarzinom .
Eine Erweiterung des Trastuzumab-Konzeptes ist die chemische Verlinkung des Antikörpers mit einer zytotoxisch wirksamen Substanz. In einer aktuell vorgestellten, randomisierten Phase III Studie war Trastuzumab-Emtansin (T-DM1) bei vorbehandelten Patientinnen dem Vergleichsarm Lapatinib/Capecitabin überlegen, siehe Studienergebnisse Mammakarzinom .
5.4.3.1 Substanzen (in alphabetischer Reihenfolge)
Lapatinib
Lapatinib ist ein oraler Tyrosinkinase-Inhibitor von HER2 und EGFR. Seine Wirksamkeit wurde bisher in der palliativen und in der neoadjuanten Situation nachgewiesen. Die Remissionsraten der Monotherapie im metastasierten Stadium liegen bei 15 - 20 %, deutlicher höher in Kombination mit Chemotherapie, Aromataseinhibitoren oder Trastuzumab. In der neoadjuvanten Therapie sind die pCR Raten möglicherweise niedriger als bei Verwendung von Trastuzumab. Charakteristische Nebenwirkung von Lapatinib ist ein Hautexanthem (Rash). Schwere Nebenwirkungen sind selten, in verschiedenen Kombinationstherapien sind Diarrhoen Grad 3/4 aufgetreten. Kritisch ist die Beeinträchtigung der linksventrikulären Funktion bis zur manifesten Herzinsuffizienz.
Pertuzumab
Pertuzumab ist ein humanisierter Anti-HER2 Antikörper. Er bindet an die Subdomäne II des extrazellulären Anteils von HER2 und verhindert die Dimerisierung mit anderen HER Rezeptoren. Die klinische Wirksamkeit wurde bisher in einer Phase III Studie bei Patientinnen mit HER2 positivem, metastasiertem Mammakarzinom gezeigt, in der Pertuzumab zusätzlich zu Trastuzumab und Docetaxel gegeben wurde. Die Dreifachkombination führte zu höheren Remissionsraten, einer Verlängerung des progressionsfreien Überlebens und zu weniger Todesfällen als die Zweifachkombination Trastuzumab / Docetaxel im Kontrollarm. Schwere Nebenwirkungen (Grad 3/4), die im Pertuzumab-Arm um mindestens 5% häufiger auftraten, waren febrile Neutropenie und Diarrhoe.
Trastuzumab
Trastuzumab ist der erste monoklonale Antikörper, der spezifisch mit dem HER2/neu-Rezeptor interferiert und für die Behandlung von Patientinnen mit HER2-Überexpression oder -Genamplifikation zugelassen wurde. Er ist wirksam in der neoadjuvanten, der adjuvanten und in der palliativen Situation. Die Remissionsraten der Monotherapie im metastasierten Stadium liegen bei 19 - 26%, in Kombination mit Chemotherapie deutlich höher. Schwere Nebenwirkungen (Grad 3/4) sind selten. Kritisch ist die Beeinträchtigung der linksventrikulären Funktion bis zur manifesten Herzinsuffizienz. Diese tritt gehäuft bei Patientinnen mit vorbestehender kardialer Erkrankung und bei gleichzeitiger Chemotherapie mit Anthrazyklinen auf.
5.4.4 Erhaltungstherapie
Realistisches Ziel bei der Behandlung von Patientinnen mit metastasiertem Mammakarzinom ist eine Remission mit Symptomlinderung und eine Verlängerung der progressionsfreien Zeit. Dagegen müssen die Nebenwirkungen und die Belastung durch die Behandlung abgewogen werden. Die palliative endokrine Therapie wird bis zum Progress fortgeführt. Die Chemotherapie wird bis zum maximalen Ansprechen durchgeführt. Für eine Erhaltungschemotherapie wurde in Einzelstudien kein konsistenter Gewinn nachgewiesen, in einer Meta-Analyse von2011 allerdings eine Verlängerung der Gesamtüberlebenszeit mit einem Hazard Ratio von 0,91.
Die Therapie mit Trastuzumab, Lapatinib oder Bevacizumab kann bis zum Progress fortgeführt werden. Ergebnisse randomisierter Phase III Studien zu diesem Vorgehen im Vergleich zu einer Intervalltherapie stehen aus.
5.4.5 Palliative Therapie - symptomorientiert
Palliative Therapie beinhaltet die Behandlung körperlicher und psychischer Beschwerden. Sie erfolgt interdisziplinär. Die Notwendigkeit und die Möglichkeiten der Palliativtherapie sollen frühzeitig und umfassend mit allen Betroffenen besprochen werden. Besondere Situationen Die folgenden, spezifischen Symptome treten besonders häufig bei Patienten mit fortgeschrittenem Mammakarzinom auf.
5.4.5.1 Knochenmetastasen
Zur Therapie von Patientinnen mit Knochenmetastasen stehen lokale und systemische Maßnahmen zur Verfügung [7, 8]. Bei Schmerzsymptomatik oder Frakturgefährdung ist die Bestrahlung die Therapie der Wahl. Eine zusätzliche Option ist die operative Versorgung bei pathologischen Frakturen, instabilen Wirbelkörperfrakturen oder als Entlastung bei spinaler Kompression. Myelon- und Nervenkompression sind Notfälle, die einer sofortigen interdisziplinären Therapie bedürfen.
Systemische Maßnahmen sind die kausale Therapie sowie die supportive Therapie mit Bisphosphonaten (Clodronat, Ibandronat, Pamidronat, Zoledronat) oder dem RANKL Antikörper Denosumab. Bisphosphonate oder Denosumab reduzieren das Risiko von skelettbezogenen Komplikationen. In einer aktuell publizierten, randomisierten Studie führte Denosumab im Vergleich mit Zoledronat zu einer signifikanten Verlängerung der Zeit bis zum Auftreten skelettbezogener Komplikationen. Die progressionsfreie und die Gesamtüberlebenszeit wurden dadurch nicht beeinflusst.
Bisphosphonate sind auch indiziert bei Tumor-induzierter Hyperkalzämie.
5.4.5.2 Hirnmetastasen
Erste Maßnahme bei symptomatischer Metastasierung ist die Gabe von Glukokortikosteroiden zur Reduktion des perifokalen Ödems. Bei einer isolierten Hirnmetastase ist eine lokale Therapie mit Operation oder stereotaktischer Bestrahlung sinnvoll. Bei multiplen Metastasen wird eine palliative Ganzhirnbestrahlung durchgeführt.
5.4.5.3 Maligner Pleuraerguss
Basierend auf einer Metaanalyse von 36 randomisierten Studien und insgesamt 1499 Patienten mit malignem Pleuraerguss hat sich die thorakoskopische Talkumpleurodese als Standard etabliert [30]. Eine ausführlichere Darstellung der verschiedenen Substanzen und Zugangswege findet sich in der Leitlinie Onkopedia Leitlinie Lungenkarzinom nichtkleinzellig (NSCLC) .
6 Rehabilitation
Der Rehabilitationsbedarf von Brustkrebspatientinnen ist hoch, sowohl aus somatischen, psychischen als auch aus sozialen Gründen einschl. ggf. Hilfen bei der beruflichen Reintegration. Die Notwendigkeit für eine Rehabilitation orientiert sich weniger an dem Tumorstadium oder der Therapie als vielmehr an den physischen und psychischen Funktionsstörungen und den sich daraus ergebenden Beeinträchtigungen. Im Bereich der Deutschen Rentenversicherung (DRV) entfiel im Jahr 2010 ein Drittel der stationären onkologischen Rehabilitationsmaßnahmen auf Patientinnen mit Mammakarzinom.
Die Patientinnen sollen über die Möglichkeiten ambulanter und stationärer Rehabilitationsmaßnahmen sowie weiterer Ansprüche, die sich aus dem Sozialrecht ergeben, informiert werden. Die Information sollte frühzeitig, d.h. vor Abschluss einer Strahlen- oder Chemotherapie, vermittelt werden. Hinsichtlich der Rehabilitationsklinik sollen die Wünsche der Patientin berücksichtigt werden (Deutschland: §9 SGB IX). Dennoch sollte eine Empfehlung für eine Klinik mit onkologischem Schwerpunkt abgegeben werden, um einen optimalen Rehabilitationserfolg zu gewährleisten.
Rehabilitationsziele werden individuell definiert. Die dabei eingesetzten Methoden waren zunächst empirisch begründet und wurden zunehmend in den letzten Jahren mit Methoden der Evidenz-basierten Medizin überprüft, sieheStudienergebnisse Mammakarzinom .
Sport- und bewegungstherapeutische Elemente haben langfristig einen positiven Effekt auf die Lebensqualität, das krankheitsspezifische Überleben und die Gesamtüberlebenszeit von Patientinnen mit Mammakarzinom.
Auch die Änderung von Ernährungsgewohnheiten in Richtung einer höheren Aufnahme von Obst und Gemüse, von ballaststoffreicherer und fettärmerer Kost kann zu einer Verbesserung des progressionsfreien Überlebens und der Gesamtüberlebenszeit führen. Die distinkte Bewertung einzelner Nahrungskomponenten und die Definitionen besonderer Zielgruppen, z. B. der Relevanz von Hitzewallungen), steht aus. Das Ziel dieser Maßnahmen ist präventiv, ebenso wie Informationen und Unterstützung zu Änderungen des Lebensstils (Rauchen, hoher Alkoholkonsum).
Psychoonkologische Begleittherapie erleichtert die Verarbeitung der Krankheitserfahrung. Ein positiver Einfluss auf das progressionsfreie und das Gesamtüberleben ist nicht gesichert.
In der Schweiz und in Österreich ist die onkologische Rehabilitation im Aufbau.
7 Nachsorge
Ein Ziel der Nachsorge ist die frühzeitige Diagnose von lokoregionären Rezidiven oder eines Zweitkarzinoms mit der Chance einer erneuten Behandlung in kurativer Intention. Weitere Ziele sind die Erkennung und Behandlung von Nebenwirkungen der Therapie, und die Fortsetzung der psychosozialen Unterstützung und Beratung. Zeitpunkte und Maßnahmen sind in Tabelle 5 zusammengefasst.
Bei Bedarf ist die Nachsorge symptomorientiert zu konzipieren. Labor- und apparative Diagnostik sind bei anamnestischem oder klinischem Verdacht auf Rezidiv oder Metastasen indiziert. Eine routinemäßige Suche nach Fernmetastasen ist aufgrund der Unsicherheit der eingesetzten Methoden und der Untersuchungsintervalle bei symptomfreien Patientinnen nicht indiziert. Alle Patientinnen mit axillärer Lymphadenektomie sollen über die Option der Erkennung, Prophylaxe und Behandlung eines Lymphödems des Arms postoperativ aufgeklärt werden (SLN = Prophylaxe). Die Einleitung einer prophylaktischen Lymphdrainage ist nicht indiziert.
Zeitpunkt (Monate) | |||||||||||||||||||||
3 | 6 | 9 | 12 | 15 | 18 | 21 | 24 | 27 | 30 | 33 | 36 | 42 | 48 | 54 | 60 | 72 | 84 | 96 | 108 | 120 | |
Anamnese, körperliche Untersuchung, Beratung | X | X | X | X | X | X | X | X | (X) | X | (X) | X | X | X | X | X | X | X | X | X | X |
Bildgebende Diagnostik der Brust1 | X | X | X | X | X | X | X | X | X | X | |||||||||||
1Standard der apparativen Diagnostik sind Mammographie und Sonographie der betroffenen sowie Mammographie der kontralateralen Brust. Die Magnetresonanztomographie wird empfohlen bei Patientinnen mit BRCA1 oder BRCA2 Mutationen, bei Zustand nach Aufbauplastiken und in der bildgebenden Differenzierung von Narbengewebe versus Zweitneoplasie.
8 Literatur
Gesellschaft der epidemiologischen Krebsregister in Deutschland / Robert - Koch Institut: Krebs in Deutschland 2005 - 2006, Häufigkeiten und Trends: Brustdrüse der Frau, 8. Auflage 2012; 64 - 67
http://www.statistik.at/web_de/statistiken/gesundheit/krebserkrankungen/brust/index.html
Deutsches Konsortium für hereditären Brust- und Eierstockskrebs; http://www.mammamia-online.de/MMSpezialBuch.pdf
Hamajima N, Hirose K, Tajima K et al.: Alcohol, tobacco and breast cancer - collaborative reanalysis of individual data from 53 epidemiological studies, including 58,515 women with breast cancer and 95,067 women without the disease. Br J Cancer 87: 1234-1245, 2002. DOI: 10.1038/sj.bjc.6600596
Puntoni M, Decensi A: The rationale and potential of cancer chemoprevention with special emphasis on breast cancer.Eur J Cancer 2009; 45 (S1):346-354. PMID:19775631
S3 - Leitlinie zur Brustkrebs-Früherkennung in Deutschland 2008, http://www.awmf.org/uploads/tx_szleitlinien/077-001_S3_Brustkrebs-Frueherkennung_lang_02-2008_02-2011.pdf
Interdisziplinäre S3-Leitlinie für die Diagnostik, Therapie und Nachsorge des Mammakarzinoms, http://www.awmf.org/uploads/tx_szleitlinien/032-045OL_l_S3__Brustkrebs_Mammakarzinom_Diagnostik_Therapie_Nachsorge_2012-07.pdf
Aebi S, Davidson T, Gruber G, Cardoso F: Primary breast cancer: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol 22 (S6): vi12-vi24, 2011. DOI: 10.1093/annonc/mdr371
AGO Kommission Mamma: Empfehlungen zur Diagnostik und Therapie des primären und metastasierten Mammakarzinoms. www.ago-online.de
Goldhirsch A, Wood WC, Coates AS et al.: Strategies for subtypes - dealing with the diversity of breast cancer: highlights of the St. Gallen International Expert Consensus on the primary therapy of early breast cancer 2011. Ann Oncol 22:1736-1747, 2011. DOI: 10.1093/annonc/mdr304
EBCTCG: Effects of radiotherapy and surgery in early breast cancer. An overview of the randomized trials. N Engl J Med 1995; 333:1444-1455.PMID: 7477144
Kühn T, Bembenek A, Decker T et al.: A concept for the clinical implementation of sentinel lymph node biopsy in patients wich breast carcinoma with special regard to quality assurance. Cancer 2005; 103:451-461. DOI: 10.1002/cncr.20786
EBCTCG: Effects of radiotherapy after breast-conserving surgery on 10-year recurrence and 15-year breast cancer death: meta-analysis of individual patient data for 10,801 women in 17 randomised trials. Lancet 378:1707-1716, 2011. PMID: 22019144
START Trialists‘s Group: The UK standardisation of breast radiotherapy (START) Trial B of radiotherapy hypofractionation for treatment of early breast cancer: a randomized trial. Lancet 2008; 371:1098-1107. DOI: 10.1016/S0140-6736(08)60348-7
Whelan TJ, Pignol JP, Levine MN et al.: Long-term results of hypofractionated radiation therapy for breast cancer.N Engl J Med 2010; 362:513-520. PMID: 20147717
Hammond ME, Hayes DF, Dowsett M et al.: American Society of Clinical Oncology/College of American Pathologists guideline recommendations for immunohistochemical testing of estrogen and progesterone receptors in breast cancer. Arch Pathol Lab Med. 2010;134:907-22. PMID: 20524868
LHRH agonists in Early Breast Cancer Overview Group: Use of luteinising-hormone agonists as adjuvant treatment in premenopausal patients with hormone-receptor-positive breast cancer: a meta-analysis of individual patient data from randomised adjuvant trials. Lancet 2007;369:1711-1723. PMID: 17512856
Early Breast Cancer Trialists‘ Collaborative Group: Relevance of breast cancer hormone receptors and other factors to the efficacy of adjuvant tamoxifen: patient-level meta-analysis of randomized trials. Lancet 378:771-784, 2011. PMID: 21802721DOI:10.1016/S0140-6736(11)60993-8
Dowsett MR, Cuzick J, Ingle J et al.: Meta-Analysis of breast cancer outcomes in adjuvant trials of aromatase inhibitors versus tamoxifen J Clin Oncol 28:509-518, 2009. DOI: 10.1200/JCO.2009.23.1274
Early Breast Cancer Trialists‘ Collaborative Group: Effects of chemotherapy and hormonal therapy for early breast cancer on recurrence and 15-year survival: an overview of the randomised trials. Lancet 2005;365:1687-1717. PMID: 15894097
Bonilla L, Ben-Aharon I, Vida L et al.: Dose-dense chemotherapy in nonmetastatic breast cancer: a systematic review and meta-analysis of randomized controlled trials. J Natl Cancer Inst 102:1845-1854, 2010.DOI:10.1093/jnci/djq409
Greil R: Is chemoendocrine treatment without alternative? Breast Care 3:231-235, 2008.DOI: 10.1159/000149558
Mauri D, Pavlidis N, Ioannidis JPA: Neoadjuvant versus adjuvant systemic treatment in breast cancer: a meta-analysis. J Nat Cancer Inst 2005;97:188-194. DOI: 10.1093/jnci/dji021
Wilcken N, Hornbuckle J, Ghersi D: Chemotherapy alone versus endocrine therapy alone for metastatic breast cancer.Cochrane Database of Systematic Reviews 2003: Issue 2. CD002747. DOI: 10.1002/14651858.CD002747
Wilcken N, Dear R: Chemotherapy in metastatic breast cancer: a summary of all randomized trials reported 2000 - 2007. Eur J Cancer 2008:44:2218-2225. DOI: 10.1016/j.ejca.2008.07.019
Beslija S, Bonneterre J, Burstein HJ et al.: Third consensus on medical treatment of metastatic breast cancer. Ann Oncol 2009;20:1771-1785. DOI:10.1093/annonc/mdp261
Carrick S, Parker S, Thornton CE et al.: Single agent versus combination chemotherapy for metastatic breast cancer.Cochrane Database of Systematic Reviews 2009:Issue 2: CD003372. DOI: 10.1002/14651858.CD003372
Cardoso F, Bedard PL, Winer EP et al.: Guidelines for management of metastastic breast cancer: combination vs sequential single-agent chemotherapy.JNCI 2009;101:1174-1181 DOI:10.1093/jnci/djp235
Oostendorp LJ, Stalmeier PF, Donders AR et al.: Efficacy and safety of palliative chemotherapy for patients with advanced breast cancer pretreated with anthracyclines and taxanes: a systematic review. Lancet Oncol 12:1053-1061, 2011. DOI:10.1016/S1470-2045(11)70045-6
Shaw PHS, Agharwal R: Pleurodesis for malignant pleural effusions.Cochrane Database of Systematic Reviews, 2004, Issue 1. DOI: 10.1002/14651858.CD002916.pub2
9 Aktive Studien
10 Medikamentöse Tumortherapie - Protokolle
Mammakarzinom - medikamentöse Tumortherapie
11 Studienergebnisse
Mammakarzinom der Frau Studienergebnisse (Phase III Studien, Metaanalysen)
12 Zulassungsstatus
Mammakarzinom - Zulassungsstatus von Medikamenten
13 Links
- www.frauenselbsthilfe.de
- www.dgho.de/gesellschaft/verein/arbeitskreise/onkologische-rehabilitation
- www.mamazone.de
14 Anschriften der Verfasser:
Ambulantes Gesundheitszentrum der Charité Universitätsmedizin Berlin
Campus Virchow Klinikum
Medizinische Klinik m. S. Hämatologie und Onkologie
Augustenburger Platz 1
13344 Berlin
Tel.: 030 / 450553219
bernhard.woermann@charite.de
Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie
Berolinahaus
Alexanderplatz 1
10178 Berlin (Mitte)
Tel.: 030 / 27 87 60 69 - 0
woermann@dgho.de
Medizinische Onkologie
Departement Medizin
Luzerner Kantonsspital
6000 Luzern 16
Tel.: +41 41 205 5860
stefan.aebi@onkologie.ch
III. Medizinische Universitätsklinik Salzburg
mit Hämatologie, Internistische Onkologie, Hämostaseologie, Infektiologie und Rheumatologie, Onkologisches Zentrum, Labor für Immunologische und Molekulare Krebsforschung (LIMCR), Center for Clinical Cancer and Immunology Trials (CCCIT)
Müllner Hauptstrasse 48
A-5020 Salzburg
Tel.: +43 / 662 / 4482 2879
r.greil@salk.at
Universität München
Brustzentrum
Frauenkliniken Maistrasse-Innenstadt und Großhadern
Marchioninistr. 15
81377 München
Tel.: 089 / 7095-7581
nadia.harbeck@med.uni-muenchen.de
Praxis und Tagesklinik für Internistische Onkologie und Hämatologie
Springstraße 24
45657 Recklinghausen
Tel.: 02361 / 90427-34
overkamp@dgho.de
Klinik Reinhardshöhe
Hämatologie/Onkologie
Quellenstr. 8-12
34537 Bad Wildungen
Tel.: 05621 / 705-154
oliver.rick@klinik-reinhardshoehe.de
Landeskrankenhaus-Universitätsklinikum Graz
Klinische Abteilung für Onkologie - Universitätsklinik für Innere Medizin
Auenbrugger Platz 15
A - 8036 Graz
Tel.: +43 / 316 / 38513115
Hellmut.Samonigg@klinikum-graz.at
Charité Universitätsmedizin Berlin
Medizinische Klinik und Poliklinik II mit Schwerpunkt Onkologie und Hämatologie
Schumannstr. 20/21
10117 Berlin
Tel.: 030 / 4505-13002
kurt.possinger@charite.de
Download
Reference:
Quellenangabe:
Onkopedia-Leitlinien werden kontinuierlich an den Stand des Wissens angepasst. Die jeweils gültige Version, AGB und Nutzungsbedingungen finden Sie unter www.onkopedia.com.
Für die kommerzielle Nutzung wenden Sie sich bitte an onkopedia@dgho.de.
Onkopedia guidelines are continuously adapted to the state of knowledge. The currently valid version, terms of use and general terms and conditions can be found at onkopedia-guidelines.info.
For commercial use, please contact onkopedia@dgho.de.




