Frühe Nutzenbewertung - Nivolumab in der neoadjuvanten Therapie des NSCLC
Die frühe Nutzenbewertung von Nivolumab ist ein weiteres Verfahren zum Einsatz beim nichtkleinzelligen Lungenkarzinom (NSCLC). Nivolumab ist zugelassen mit platinbasierter Chemotherapie für die neoadjuvante Therapie des resezierbaren NSCLC mit Tumorzell-PD-L1-Expression >1% und hohem Rezidivrisiko. Der G-BA hat das IQWiG mit dem Bericht beauftragt. Pharmazeutischer Unternehmer und IQWiG kommen zu unterschiedlichen Bewertungen. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG
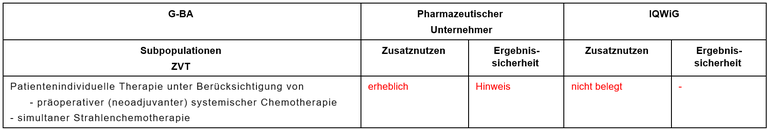
Unsere Anmerkungen sind:
- Die Festlegung einer patientenindividuellen, platinbasierten, neoadjuvanten Chemotherapie ist eine angemessene ZVT.
- Basis der frühen Nutzenbewertung ist CheckMate 816, eine initial dreiarmige Studie. Im Dossier werden die zulassungskonformen Pat. mit positiver PD-L1-Expression in den Armen Chemotherapie vs Chemotherapie + Nivolumab ausgewertet. Diese Population besteht aus 178 Pat.
- Die Hinzunahme von Nivolumab führte zur signifikanten Steigerung der Rate pathohistologischer Komplettremissionen, zur Verlängerung des ereignisfreien Überlebens, zur Verlängerung der Gesamtüberlebenszeit und zur Erhöhung der Überlebensrate nach 36 Monaten.
- Die Rate unerwünschter Ereignisse wurden durch Nivolumab nicht signifikant gesteigert.
- Die Zulassungsstudie hat methodische Schwächen:
- Die Studie war nicht auf den Endpunkt „Gesamtüberleben“ gepowert.
- Die Ergebnisse der Operation (R0-Rate) sind niedriger als in der deutschen Versorgung.
- Die Rate von Pat. im Kontrollarm mit Gabe von Immuncheckpoint-Inhibitoren im Rezidiv erscheint relativ niedrig.
- Die Analysen zu Lebensqualität und Patient-Reported-Outcome sind dürftig.
- Die Aussagen zugunsten von Nivolumab können nicht auf Pat. übertragen werden, die für eine definitive Strahlenchemotherapie geeignet sind.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Chemotherapie + Nivolumab den Grad A (Skala A (hoch) – C (niedrig).
Trotz der methodischen Kritikpunkte sind die Ergebnisse von CheckMate 816 beeindruckend und wurden in dieser Ausprägung in diesem Patientenkollektiv bisher nicht erreicht. Bei Pat. mit Indikation zur neoadjuvanten Therapie und mit Expression von PD-L1 >1% und hohem Rezidivrisiko gehört die Hinzunahme von Nivolumab (oder zukünftig auch anderer Immuncheckpoint-Inhibitoren) zum neuen Therapiestandard.



