Frühe Nutzenbewertung - Olaparib beim Mammakarzinom - adjuvant
Die frühe Nutzenbewertung von Olaparib (Lynparza®) ist das erste Verfahren zur adjuvanten Therapie des Mammakarzinoms bei Patientinnen und Patienten (Pat.) mit BRCA-Keimbahnmutationen. Olaparib ist indiziert als Monotherapie oder in Kombination mit einer endokrinen Therapie bei Pat. mit Keimbahn-BRCA1/2-Mutationen, die ein HER2-negatives Mammakarzinom im Frühstadium mit hohem Rezidivrisiko haben und zuvor mit neoadjuvanter oder adjuvanter Chemotherapie behandelt wurden. Der G-BA hat keine Subgruppen gebildet. Das IQWiG wurde mit dem Bericht beauftragt. Pharmazeutisches Unternehmen und IQWiG kommen zu unterschiedlichen Bewertungen. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle 1: Vorschläge zum Zusatznutzen von Olaparib
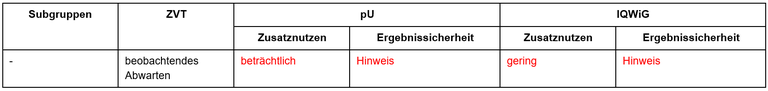
Legende: pU – pharmazeutischer Unternehmer, ZVT – zweckmäßige Vergleichstherapie
Unsere Anmerkungen sind:
- Die festgelegte, zweckmäßige Vergleichstherapie entspricht dem Standard bei Pat. nach neoadjuvanter bzw. adjuvanter Chemotherapie. Die Fortsetzung der endokrinen Therapie bei der kleinen Gruppe von HR+ Pat. ist sinnvoll.
- Basis der frühen Nutzenbewertung ist die internationale, randomisierte, Placebo-kontrollierte Phase-III-Studie OlympiA zum Vergleich von Olaparib vs Placebo.
- Olaparib führte zu einer signifikanten Steigerung der krankheitsfreien und der Gesamtüberlebensrate. Der Median der Überlebenszeit war in beiden Studienarmen noch nicht erreicht.
- Die Rate schwerer unerwünschter Ereignisse lag unter Olaparib viel höher als im Placebo-Arm. Die Mehrzahl der Nebenwirkungen ist hämatologisch und beschränkt sich auf Laborveränderungen. Die Lebensqualität wurde durch die Nebenwirkungen nicht beeinträchtigt.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Olaparib den Grad A (Skala A (hoch) – C (niedrig)).
Die ergänzende adjuvante Therapie mit Olaparib über ein Jahr ist der neue Standard bei Pat. mit frühem, gBRCAmut Mammakarzinom und erhöhtem Rezidivrisiko, definiert durch eine fehlende pathohistologische Komplettremission nach neoadjuvanter Therapie oder durch etablierte Risikofaktoren nach der TNM-Klassifikation.



