Frühe Nutzenbewertung - Abemaciclib beim HR+/HER2- metastasierten Mammakarzinom, Kombination mit Fulvestrant
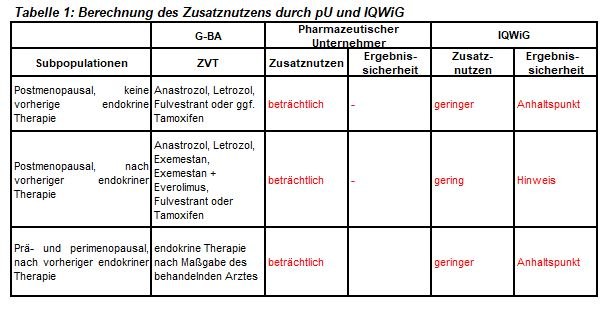
Abemaciclib ist zugelassen zur Therapie von Patientinnen mit Hormonrezeptor (HR)-positivem, HER2-negativem, lokal fortgeschrittenem oder metastasiertem Mammakarzinoms, die noch keine initiale endokrine Therapie erhalten haben, und für Patientinnen nach vorangegangener endokriner Therapie. Die erneute Nutzenbewertung bezieht sich ausschließlich auf die Kombination mit Fulvestrant. Das IQWiG wurde mit dem Bericht beauftragt. Subgruppen, zweckmäßige Vergleichstherapie sowie die unterschiedlichen Bewertungsvorschläge sind in Tabelle 1 zusammengefasst.
Unsere Anmerkungen sind:
- Die Bildung von Subgruppen auf der Basis von Erst- und Zweitlinientherapie und aufgrund des Menopausenstatus ist biologisch und medizinisch nur schlecht begründbar. Bei Einsatz derselben Arzneimittel ist ein spätes Rezidiv unter adjuvanter endokriner Therapie therapeutisch nicht wesentlich anders als ein Rezidiv unter endokriner Therapie in der initialen, metastasierten Phase zu bewerten. Viele, als prä- und perimenopausal klassifizierte Patientinnen sind funktionell postmenopausal durch den parallelen Einsatz von GnRH-Analoga.
- Basis der frühen Nutzenbewertung zum Vergleich von Fulvestrant + Abemaciclib vs Fulvestrant bei den postmenopausalen Patientinnen ist die multizentrische, randomisierte Phase-III-Studie MONARCH 2.
- Die Kombination von Fulvestrant + Abemaciclib führt gegenüber Fulvestrant zur Steigerung der Remissionsrate, zur Verlängerung der progressionsfreien Überlebenszeit und nach längerer Nachbeobachtung zur statistisch signifikanten Verlängerung der Gesamtüberlebenszeit.
- Die Lebensqualität war in den beiden Studienarmen nicht signifikant unterschiedlich.
- Die Rate schwerer, Therapie-assoziierter Nebenwirkungen ist im Abemaciclib-Arm viel höher als im Kontroll-Arm. Die häufigste Nebenwirkung unter Abemaciclib ist die Diarrhoe. Hier ist ein differenziertes Nebenwirkungsmanagement entsprechend der Fachinformation erforderlich.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Abemaciclib in Kombination mit Fulvestrant den Grad 4 (Skala 1 (niedrig) – 5 (hoch)).
CDK4/6 Inhibitoren sind inzwischen Standard in der endokrin-basierten Therapie des fortgeschrittenen und metastasierten Mammakarzinoms. Bezüglich der Verlängerung der Gesamtüberlebenszeit zeigt sich jetzt auch in MONARCH 2 ein signifikanter Unterschied zugunsten von Abemaciclib.
Zur Stellungnahme