Frühe Nutzenbewertung - Nivolumab beim Ösophaguskarzinom
Diese frühe Nutzenbewertung von Nivolumab (Opdivo®) betrifft eine weitere Indikation zum Einsatz dieses Immuncheckpoint-Inhibitors und ist das erste Verfahren zu einem neuen Arzneimittel beim Ösophaguskarzinom. Nivolumab ist als Monotherapie zur Behandlung des nicht resezierbaren, fortgeschrittenen, rezidivierten oder metastasierten Plattenepithelkarzinoms des Ösophagus bei Erwachsenen nach vorheriger fluoropyrimidin- und platinbasierter Kombinationschemotherapie indiziert. Das IQWiG wurde mit dem Bericht beauftragt. Subgruppen, zweckmäßige Vergleichstherapie sowie die unterschiedlichen Bewertungsvorschläge sind in Tabelle 1 zusammengefasst.
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG
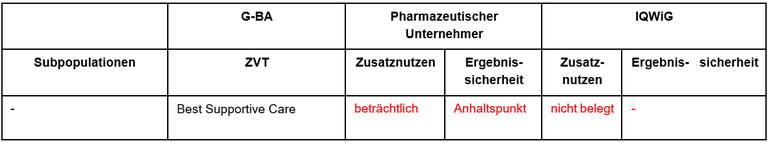
Unsere Anmerkungen sind:
- Zweckmäßige Vergleichstherapie ist eine Therapie nach Maßgabe des behandelnden Arztes unter Berücksichtigung von Allgemeinzustand und Komorbidität, Ansprechen auf Vortherapie und Patientenwunsch. Basis in dieser Behandlungssituation ist Best Supportive Care. Ergänzend eingesetzte Zytostatika sind vor allem Taxane (Docetaxel oder Paclitaxel), in Einzelfällen auch Irinotecan sowie Bestandteile der Erstlinientherapie, wenngleich beide Alternativen mit deutlich weniger Daten und Erfahrungen belegt sind als eine Zweitlinientherapie mit Taxanen. In Patienten mit gutem Allgemeinzustand wird eine zytostatische Therapie Standard in Deutschland angewandt.
- Basis der frühen Nutzenbewertung zum Vergleich von Nivolumab vs Taxane ist die randomisierte, offene Phase-III-Studie ATTRACTION-3. 96% der Patient*innen kamen aus dem asiatischen Raum.
- Nivolumab führte gegenüber Taxanen zu einer statistisch signifikanten Verlängerung der Gesamtüberlebenszeit (HR 0,77; Median 2,5 Monate, absoluter Unterschied 13% nach 12 Monaten, 10% nach 18 Monaten). Die Ansprechraten waren gleich, die progressionsfreie Überlebenszeit nicht unterschiedlich.
- Die Rate schwerer, Therapie-assoziierter Nebenwirkungen war im Nivolumab-Arm viel niedriger als im Kontroll-Arm (18 vs 63%). Die Rate von Therapieabbrüchen war in den beiden Studienarm vergleichbar.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Nivolumab den Grad 4 (Skala 1 (niedrig) – 5 (hoch)).
Nivolumab ist das erste, in den letzten 10 Jahren neu zugelassene Arzneimittel beim fortgeschrittenen Plattenepithelkarzinom des Ösophagus. Es ist eine neue Option mit klinischem Nutzen bei Patient*innen mit Plattenepithelkarzinom nach systemischer Vortherapie.
Aufgrund der niedrigen Zahl von Patient*innen aus dem europäischen Raum in der Zulassungsstudie kann der Zusatznutzen für diese Subpopulation nicht zuverlässig quantifiziert werden.



