Frühe Nutzenbewertung - Trastuzumab Deruxtecan beim HER2-positiven Mammakarzinom
Die frühe Nutzenbewertung von Trastuzumab Deruxtecan (Enhertu®) ist ein weiteres Verfahren zur Therapie des HER2-positiven Mammakarzinoms und das erste Verfahren zu diesem Antikörper-Drug-Konjugat. Trastuzumab Deruxtecan ist zugelassen zur Monotherapie von Patientinnen und Patienten (Pat.) mit inoperablem oder metastasiertem HER2-positivem Brustkrebs, die bereits mindestens eine gegen HER2 gerichtete Vorbehandlung erhalten haben. Der G-BA hat keine Subgruppen gebildet. Das IQWiG wurde mit dem Bericht beauftragt. Pharmazeutisches Unternehmen und IQWiG kommen zu unterschiedlichen Bewertungen. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle 1: Vorschläge zum Zusatznutzen von Trastuzumab Deruxtecan
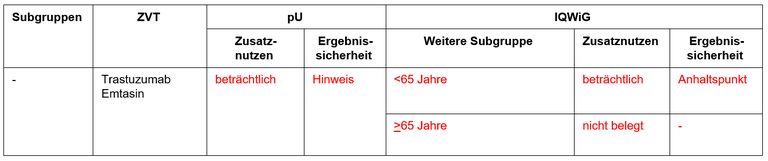
Legende: pU – pharmazeutischer Unternehmer, ZVT – zweckmäßige Vergleichstherapie
Unsere Anmerkungen sind:
- Die festgelegte, zweckmäßige Vergleichstherapie entspricht dem Standard bei Pat., die für eine gezielte Therapie mit PARP- oder Immuncheckpoint-Inhibitoren nicht geeignet sind.
- Basis der frühen Nutzenbewertung ist die internationale, randomisierte Phase-III-Studie DESTINY-Breast03 zum Vergleich von Trastuzumab Deruxtecan vs Trastuzumab Emtansin.
- Trastuzumab Deruxtecan führte zu einer signifikanten Steigerung der Remissionsrate, zur Verlängerung des progressionsfreien Überlebens sowie der Gesamtüberlebenszeit.
- Die Rate schwerer unerwünschter Ereignisse lag unter Trastuzumab Deruxtecan etwas höher als unter Trastuzumab Emtansin. Besonders zu beachten sind das erhöhte Risiko für eine Neutropenie, Übelkeit und Erbrechen sowie das mögliche Auftreten einer Pneumonitis.
- Im IQWiG-Bericht wird eine Subgruppenbildung aufgrund des Alters vorgeschlagen. Für Pat. im Alter >65 Jahre sei der Zusatznutzen nicht belegt. Dieser Vorschlag ist aufgrund der geringen Zahl von Ereignissen in dieser Altersgruppe (n=15) nicht gut begründet. Darüber hinaus sind die Unterschiede in der Ansprechrate und beim progressionsfreien Überleben zugunsten von Trastuzumab Deruxtecan nicht unterschiedlich zwischen jüngeren und älteren Pat.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Trastuzumab Deruxtecan den Grad 3 (Skala 1 (niedrig) – 5 (hoch)).
Aufgrund der Daten von DESTINY-Breast 03 löst Trastuzumab Deruxtecan den bisherigen Standard Trastuzumab Emtansin als neuen Standard in dieser Indikation ab.
Zur Stellungnahme für eine Vortherapie



