Frühe Nutzenbewertung - Dostarlimab beim Endometriumkarzinom
Diese frühe Nutzenbewertung von Dostarlimab (Jemperli®) ist das erste Verfahren zu einem neuen Arzneimittel beim Endometriumkarzinom. Dostarlimab ist ein PD-1-Inhibitor und zugelassen für die Behandlung von Patientinnen mit rezidivierendem oder fortgeschrittenem Endometriumkarzinom und Mismatch-Reparatur-Defizienz (dMMR)/hoher Mikrosatelliteninstabilität (MSI-H) im Progress während oder nach einer vorherigen Behandlung mit einer Platin-basierten Therapie. Das IQWiG wurde mit dem Bericht beauftragt. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG
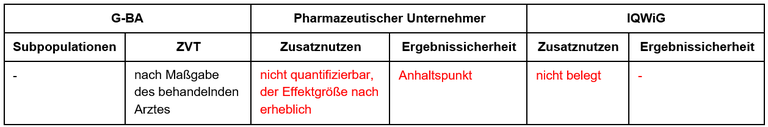
Unsere Anmerkungen sind:
- Die vom G-BA festgelegte, zweckmäßige Vergleichstherapie (ZVT) ist eine Therapie nach Maßgabe des behandelnden Arztes. Dies entspricht den Empfehlungen der Fachgesellschaften.
- Basis der frühen Nutzenbewertung ist GARNET, eine offene Phase-I-Studie.
- Dostarlimab führte zu einer Remissionsrate von 37% und einer medianen progressionsfreien Überlebenszeit von 5,6 Monaten. Die Progressionsrate nach 8 Monaten ist sehr niedrig. Der Median der Überlebenszeit wurde noch nicht erreicht.
- Das Spektrum der Nebenwirkungen ist substanzklassenspezifisch.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Dostarlimab den Grad 3 (Skala 1 (niedrig) – 5 (hoch)).
Aufgund der neuesten Entwicklungen in der Molekularpathologie hat sich das Verständnis zur Tumorbiologie beim Endometriumkarzinom erheblich verändert. Beim rezidivierten Endometriumkarzinom nach platinhaltiger Chemotherapie besteht ein sehr großer und bisher ungedeckter Bedarf an medikamentöse Therapien, da die aktuell eingesetzten Systemtherapien in ihrer Wirksamkeit sehr limitiert sind. Mit Dostarlimab steht nun der erste Immuncheckpoint-Inhibitor in dieser Indikation bei Nachweis von MSI-H/dMMR zur Verfügung. Die Ergebnisse von Dostarlimab liegen weit über denen der bisherigen Therapiemöglichkeiten.
Mangels direkt vergleichender Daten ist der Nutzen von Dostarlimab schwer quantifizierbar, da die Studien, auf denen die aktuellen medikamentösen Standardtherapien, inklusive den Chemotherapien, ohne die Erkenntnisse der MSI-Testung erfolgten. Die üblicherweise indizierten, medikamentösen Therapien (u.a. Doxorubicin) zeigen in den Phase-III Studien sehr mäßige Effektivität in der Gesamtpopulation des Endometriumkarzinoms (inklusiv MSI-L/pMMR sowie MSI-H/dMMR). In der aktuellen Europäischen Leitlinie /ESGO/ESTREL) wird die Testung zwecks Optimierung der Therapieentscheidung bei Patientinnen mit Endometriumkarzinom eingefordert (ESGO/ESMO/ESTRO), die deutsche S3-Leitlinie wird dies in ihrer Aktualisierung (Erscheinungstermin im Januar 2022) ebenfalls als Standard deklarieren.



